下列溶液中,各微粒的物质的量浓度关系正确的是
| A.室温下,向0.01 mol·L-1的NH4HSO4溶液中滴加NaOH溶液至中性:C(Na+)>C(SO42-)>C(NH4+)>C(OH-)=C(H+) |
| B.0.1 mol·L-1的NaHCO3溶液:C(Na+)>C(OH-)>C (HCO3-)>C(H+) |
| C.Na2CO3溶液:C(OH-)-C(H+)=C(HCO3-)+C(H2CO3) |
| D.25℃时,浓度均为0.1 mol·L-1的CH3COOH、CH3COONa混合溶液,呈酸性:C(CH3COO-)+C(OH-)<C(CH3COOH)+C(H+) |
下列除杂分离方法正确的是
| 选项 |
物质 |
杂质 |
所用试剂 |
分离方法 |
| A |
苯 |
苯酚 |
足量浓溴水 |
过滤 |
| B |
CH3CH2OH |
CH3COOH |
足量CaO |
蒸馏 |
| C |
C2H5Br |
Br2 |
足量Na2SO3(aq) |
分液 |
| D |
KCl |
CaCl2 |
足量Na2CO3溶液、盐酸 |
过滤 |
某地区的雾霾经收集处理后得试样溶液,可能含有如下离子:Na+、NH4+、Mg2+、Al3+、SO42-、NO3-、Cl-。某同学设计并完成了如下实验: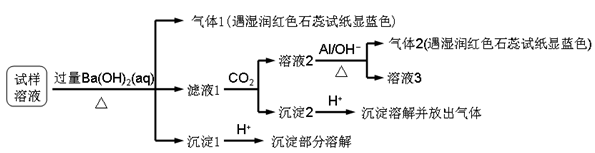
已知:3NO3-+ 8Al+5OH-+2H2O 3NH3↑+8AlO2-
3NH3↑+8AlO2-
根据以上的实验操作与现象,该同学得出的结论不正确的是
| A.试样中肯定存在NH4+、Mg2+、SO42-和NO3- |
| B.试样中一定不含Al3+ |
| C.试样中可能存在Na+、Cl- |
| D.该雾霾中可能存在NaNO3、NH4Cl和MgSO4 |
化学与社会、生活密切相关。对下列现象或事实的解释正确的是
| 选项 |
现象或事实 |
解 释 |
| A |
用热的纯碱溶液洗去油污 |
Na2CO3可直接和油污反应 |
| B |
漂白粉在空气中久置变质 |
漂白粉中的CaCl2与空气中的CO2反应生成CaCO3 |
| C |
Ca(OH)2溶液能溶解难溶的杂卤石(K2SO4•MgSO4•2CaSO4•2H2O)浸出K+ |
氢氧根离子与镁离子结合,使平衡向右移动 |
| D |
FeCl3溶液可用于铜质印刷线路板制作 |
FeCl3能从含有Cu2+的溶液中置换出铜 |
向饱和澄清石灰水中加入少量CaC2,充分反应后立即测定所得溶液中离子浓度,下列预测正确的是
| A.c(Ca2+)、c(OH―)一定增大 | B.c(Ca2+)、c(OH―)一定保持不变 |
| C.c(Ca2+)、c(OH―)均可能减小 | D.c(OH―)增大、c(H+)减小 |
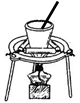
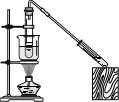
中学实验室为完成下列实验通常选择的装置正确的是
| A |
B |
C |
D |
|
| 实验 |
用CCl4萃取 溴水中的溴 |
从NaCl与I2的混合物中回收I2 |
制备与收集二氧化硫 |
制备乙酸丁酯 |
| 装置 |
 |
 |
 |
 |