相同物质的量的Na2O2和Na2O的比较中,不正确的是
A. 两种物质所含原子个数之比为4∶3 两种物质所含原子个数之比为4∶3 |
| B.两种物质所含离子个数之比为4∶3 |
| C.两种物质与足量的CO2反应,消耗气体的质量比为1∶1 |
| D.两种物质与等质量且足量的水反应得到溶液的质量分数之比为1∶1 |
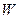 g某元素(无同位素)所含原子数目为
g某元素(无同位素)所含原子数目为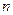 ,该元素原子的摩尔质量为
,该元素原子的摩尔质量为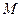 g/mol ,则氯元素的一种同位素
g/mol ,则氯元素的一种同位素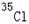 的一个原子的质量是( )(注:该Cl原子的相对原子质量≈35)
的一个原子的质量是( )(注:该Cl原子的相对原子质量≈35)
A.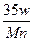 g g |
B.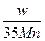 g g |
C.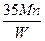 g g |
D.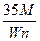 g g |
下列除去杂质的方法正确的是()
| A.除去CO2中的少量SO2:先将气体通入饱和Na2CO3溶液,再收集剩余气体 |
| B.除去NaHCO3溶液中混有的少量Na2CO3(Na2CO3摩尔质量较大):通过蒸馏,收集蒸馏产物 |
| C.除去FeCl3溶液中混有的少量AlCl3溶液:加入足量的NaOH溶液,充分反应后,过滤,向沉淀中加盐酸使其恰好完全溶解 |
D.除去碘水中的I2:加 入乙醇进行多次萃取,留在分液漏斗中的即为较纯净的水 入乙醇进行多次萃取,留在分液漏斗中的即为较纯净的水 |
判断下列说法正确的是()
| A.1molFeCl3跟水完全反应转化为氢氧化铁胶体,其中胶体粒子的物质的量为1mol |
| B.一定温度下,1L0.50mol/L NH4Cl 溶液与2L0.25mol/LNH4Cl溶液含有的NH4+的物质的量不同 |
| C.配制480mL 0.5mol/L 的CuSO4溶液,需要称取60.0g的CuSO4·5H2O晶体 |
| D.10mL质量分数为98% 的H2SO4溶液,用水稀释至100mL溶质质量分数变为9.8% |
(注:硫酸溶液的密度随浓度的增大而增大)
已知阿伏伽德罗常数为NA,下列说法中正确的是()
| A.常温常压下,当活泼金属转移2NA电子时,可从盐酸中置换产生22.4L H2 |
| B.100g98% 的浓硫酸中含有氧原子个数为4NA |
| C.CO与N2具有相同的电子总数,那么1molN2和22.4L的 CO气体所含有的电子总数为28NA |
| D.室温下,21.0g乙烯和丁烯(C4H8)的混合气体中含有的碳原子数目是1.5NA |
下列离子反应方程式改写的化学方程式正确的是( )
| A.Mg2++2OH-=Mg(OH)2↓ MgCO3+2NaOH=Mg(OH)2↓+Na2CO3 |
| B.Ba2++SO4 2 -=BaSO4↓ Ba(OH)2+H2SO4=BaSO4↓+2H2O |
| C.Ca2++OH -+HCO3 - =CaCO3↓+H2O Ca(HCO3)2+2NaOH=CaCO3↓+2H2O+Na2CO3 |
| D.Cu +2Fe3+=Cu2++2Fe2+ Cu +2FeCl3=2FeCl2+CuCl2 |