(12分)(1)物质的量浓度相同的下列物质的溶液①NH4Cl ②NH4HSO4 ③CH3COONH4,c(NH4+)由小到大的顺序是 (填序号)。
(2)同浓度的下列溶液:①CH3COONH4 ②NH4Cl ③Na2CO3 ④NaHCO3,其中pH由大到小的顺序 是 。
(3)物质的量浓度相同的 ①盐酸、②硫酸溶液、 ③醋酸(CH3COOH)溶液各100 mL分别与足量的Zn反应,在相同的条件下,产生H2的体积分别为V1、V2、V3,它们由大到小的顺序是 。
(4)CH3COONa溶液呈 性(填“酸”、“碱”或“中”),其原因是 (用离子方程式表示)。
(5)常温时,若10体积pH1=a的盐酸溶液与1体积pH2=b的氢氧化钠溶液混合后溶液呈中性,则混合前该强酸的pH1与强碱的pH2之间应满足的关系是_________________。
(共14分)A、B、C、D 四种元素,A元素所处的周期数、主族序数、原子序数均相等;B的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层少2个;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C.
(1)B元素的名称:;B在周期表中的位置第周期,第族;
(2)A、B形成的化合物为化合物;(离子化合物还是共价化合物)
(3)C的元素符号:,C的最高价氧化物的化学式:;
(4) D的最高价氧化物对应的水化物的化学式:。
已知和碳元素同主族的X元素位于元素周期表中的第一个长周期,短周期元素Y原子的最外层电子数比内层电子总数少3,它们形成化合物的分子式是XY4。试回答:
(1)、X的元素名称为:;X元素的原子基态时电子排布式为:;Y的元素符号是:;Y元素原子价层电子的电子排布图是:。
(2)、若X、Y两元素电负性分别为2.1和2.85,试判断XY4中X与Y之间的化学键为:
(填“共价键”或“离子键” )。
(3)、该化合物的孤电子对数为:;价层电子对数是:;空间构型为:;中心原子的轨道杂化类型为:;该分子为:(填“极性分子”或“非极性分子” )。
(4)、该化合物在常温下为液体,该液体微粒间的作用力为:。
(5)、该化合物的沸点与SiCl4比较:的沸点高(填化学式),原因是:
。
短周期主族元素A、B、C、D的原子序数依次增大,其中A、C同主族,B、C、D同周期,A原子的最外层的电子数是次外层电子数的3倍,B是短周期元素中原子半径最大的主族元素。试回答下列问题:
(1)、A的元素符号:;D的原子结构示意图:;C原子的核外电子排布式:;B2A2的电子式:;
A的价电子排布图:。
(2)、A、B、C三种元素形成的简单离子的半径由大到小的顺序是(用离子符号表示):
。
(3)、CA2与D元素的单质在水溶液中反应得化学方程式是:。
配合物[Ag(NH3)2]OH的中心离子是:;配体是:;配位数是:;外界是:;内界是:;该配合物发生电离的电离方程式为:。
无水CoCl2为深蓝色,吸水后变为粉红色的水合物,水合物受热后又变为CoCl2,故常在实验室用作吸湿剂和空气湿度指示剂。CoCl2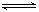 CoCl2·xH2O现有65g无水CoCl2,吸水后变成CoCl2·xH2O 119g。(1)水合物中x=;(2)、若该化合物中Co2+的配位数为6,而且经测定得知内界和外界Cl-的个数比为1:1,则其化学式可表示为:
CoCl2·xH2O现有65g无水CoCl2,吸水后变成CoCl2·xH2O 119g。(1)水合物中x=;(2)、若该化合物中Co2+的配位数为6,而且经测定得知内界和外界Cl-的个数比为1:1,则其化学式可表示为: