下列解释事实的方程式错误的是
A.测得0.1 mol·L-1氨水的pH为11:NH3·H2O NH4++OH- NH4++OH- |
| B.将Na块投入水中,产生气体:2Na+2H2O=2NaOH+H2↑ |
C.用CuCl2溶液做导电实验,灯泡发光:CuCl2 Cu2++2Cl- Cu2++2Cl- |
D.将1 mol·L-1FeCl3溶液滴入沸水中,得到透明红褐色液体:FeCl3+3H2O Fe(OH)3(胶体)+3HCl Fe(OH)3(胶体)+3HCl |
化学是一门以实验为基础的学科,掌握基本实验方法和操作技能是做好化学实验的基础。下列有关化学实验基本知识的描述不正确的是
| A.丁达尔现象可用于区别FeCl3饱和溶液和Fe(OH)3胶体 |
| B.过滤和蒸发操作中均用到玻璃棒,但玻璃棒的作用不相同 |
| C.验证烧碱溶液中是否含有Cl-,先加稀硝酸除去OH-,再加入AgNO3溶液,有白色沉淀,证明含Cl- |
| D.检验某溶液中是否含有SO42-的方法是先向该溶液中加入BaCl2溶液,再加入稀HNO3 |
用玻棒蘸取新制氯水滴在pH试纸中部,观察到的现象是()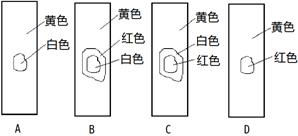
下列反应的离子方程式正确的是
A.氯气通入水中: Cl2+H2O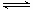 2H++Cl-+ClO- 2H++Cl-+ClO- |
| B.过氧化钠投入水中:2O22-+ 2H2O = 4OH-+ O2↑ |
| C.AlCl3溶液中加入过量氨水: Al3++4OH-= AlO2-+2H2O |
| D.少量二氧化碳通入“水玻璃”中:CO2 + SiO32― + H2O = CO32―+ H2SiO3↓ |
下列说法正确的是
| A.水晶项链和餐桌上的瓷盘都是硅酸盐制品 |
| B.工艺师可用盐酸刻蚀玻璃制作工艺品 |
| C.Si可用于信息存储,SiO2可用于光纤通讯 |
| D.由石英沙制备纯硅不涉及氧化还原反应 |
下列叙述错误的是
| A.摩尔质量的单位是g·mol-1 | B.硫原子的结构示意图: |
| C.过氧化钠必须密闭保存 | D.加碘食盐中添加的一般是KIO3 |