【化学——选修3物质结构与性质】已知A、B、C、D、E、F为前四周期的六种元素,原子序数依次增大,其中A位于周期表的s的区,其原子中电子层数和未成对电子数相同;B原子价电子排布式为nsnnpn,B和E同主族,D原子的最外层电子数是其内层的3倍;F元素位于元素周期表的第四行、第十一列。试回答下列问题:
(1)基态F原子的核外电子排布式为 。
(2)关于B2A2的下列说法中正确的是____ (填选项序号)。
①B2A2中的所有原子都满足8电子稳定结构
②每个B2A2分子中 键和
键和 键数目比为1:1
键数目比为1:1
③B2A2是由极性键和非极性键构形成的非极性分子
④B2A2中心原子的杂化类型为sp杂化
(3)B、C、D三种元素第一电离能按由大到小的顺序排列为 (用元素符号表示)。
(4)C的气态氢化物与C的最高价氧化物对应的水化物反应生成一种盐H,H晶体中存在的化学键类型
有____(填选项序号)。
①离子键 ②共价键 ③氢键 ④配位键 ⑤金属键
(5)基态E原子的最高能层具有的原子轨道数为____ ;B和E分别与氧元素形成的最高价氧化物中,熔沸点较高的是 (写化学式);
(6)F单质的晶体堆积方式为面心立方,其配位数为 ;若F的相对分子质量为M,它的晶胞棱长为a(cm),则F晶体的密度为 g·cm-3。(阿伏伽德罗常数为NA)
与下列装置相关的说法中不正确的是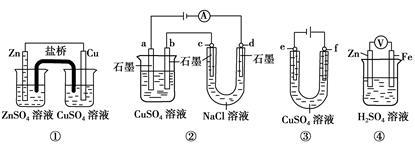
| A.装置①中,盐桥中的K+移向CuSO4溶液 |
| B.装置②中b极析出6.4 g固体时,d极产生2.24 L H2 |
| C.用装置③精炼铜时,f极为粗铜 |
| D.装置④中电子沿导线由Zn流向Fe,Fe极上有大量气泡生成 |
海水总量极大,金、铀等微量元素在海水中的总量自然也大,但从海水中获取这些微量元素的成本很高。其中成本最高的步骤在于
| A.从海水中富集含微量元素的化合物 |
| B.使含微量元素的离子沉淀 |
| C.对含微量元素的混合物进行提纯 |
| D.从化合物中冶炼这些单质 |
化学与能源开发、环境保护、生产生活等密切相关。下列说法正确的是
| A.开发利用可燃冰是缓解能源紧缺的唯一途径 |
| B.将废电池深埋,可以避免其中的重金属污染 |
| C.“地沟油”对人体的危害极大,严禁用做食用油 |
| D.食品保鲜膜、食品袋的主要成分都是聚氯乙烯 |
在三个密闭容器中分别充入A、B、C三种气体,当它们的温度和密度都相同时,这三种气体的压强(p)从大到小的顺序为p(B)>p(A)>p(C),则A、B、C分别是
A.Ne、H2、O2B.O2、N2、H2
C.NO、CO2、H2D.NH3、O2、NO2
ag镁铝合金投入x mL 2mol/L的盐酸中,金属完全溶解,再加入y mL 1mol/L的NaOH溶液,沉淀达到最大值,质量为(a+1.7)g ,则下列说法不正确的是
| A.镁铝合金与盐酸反应转移电子数为0.1NA | B.产生的H2在标况下体积为1.12L |
| C.x一定等于50 | D.a的取值范围为0.9<a<1.2 |