下列离子方程式正确的是
| A.铜溶于稀硝酸:Cu+2H++NO3-=Cu2++NO2↑+H2O |
| B.用KIO3氧化酸性溶液中的KI:5I-+IO3-+3H2O=3I 2+6OH- |
| C.向NaAlO2溶液中通入过量的CO2:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32- |
D.向新制Cu(OH)2悬浊液中加入乙醛溶液并加热:CH3CHO+2Cu(OH)2+OH- CH3COO-+Cu2O↓+3H2O CH3COO-+Cu2O↓+3H2O |
下列关于非金属元素C、N、Si、S、Cl的叙述正确的是()
A.在通常情况下它们的单质均为气体
B.每一种元素都只能形成一种单质
C.它们的最高价氧化物的水化物都属于酸
D.它们的氢化物的水溶液都显酸性
下列关于有机物 的描述正确的是()
的描述正确的是()
| A.只有1种结构 |
| B.是平面型分子 |
| C.有2种同分异构体 |
| D.有4种同分异构体 |
下列说法不正确的是()
| A.绿色化学的核心就是在生产过程中减少污染 |
| B.水华、赤潮等水体污染是由于含氮、磷的大量污水任意排放造成的 |
| C.形成酸雨的主要物质是硫氧化物和氮氧化物(NOx) |
| D.大气污染物主要来自化石燃料燃烧和工业生产过程中产生的废气 |
X和Y的原子序数都小于18,两者能组成化合物X2Y3,已知X的原子序数为n,则Y的原子序数不可能是()
| A.n+11 | B.n-5 | C.n+3 | D.n-6 |
mol气态钠离子和1mol气态氯离子结合生成1mol氯化钠晶体释放出的热能为氯化钠晶体的晶格能。下列热化学方程中,能直接表示出氯化钠晶体格能的是()
| A.Na+(g)+Cl-(g) |
B.Na(s)+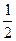 Cl2(g) Cl2(g) |
| C.Na(s) |
D.Na(g)-e- |