下列叙述正确的是
| A.常温时,某溶液中由水电离出来的c(H+)和c(OH-)的乘积为1×10-24,该溶液中一定可以大量存在:K+、Na+、AlO2-、SO42- |
| B.常温时,0.1mol/LHA溶液的pH>1,0.1mol/LBOH溶液中c(OH-)/c(H+)=1012,将这两种溶液等体积混合,混合后溶液中离子浓度的大小关系为: c(B+)>c(OH-)>c(H+)>c(A-) |
| C.过量SO2通入到Ba(NO3)2溶液中,离子反应方程式为: 3SO2+2NO3-+3Ba2++2H2O  3BaSO4↓+2NO↑+4H+ 3BaSO4↓+2NO↑+4H+ |
| D.用pH=3和pH=2的醋酸溶液中和含等量NaOH的溶液所消耗的醋酸溶液的体积分别为Va和Vb,则Va>10Vb |
氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如右图。下列有关氢氧燃料电池的说法正确的是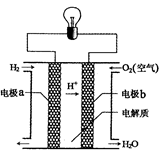
| A.该电池的总反应:2H2+O2=2H2O |
| B.该电池中电极b是负极 |
| C.外电路中电子由电极b通过导线流向电极a |
| D.该电池工作时电能转化为化学能 |
既可用来鉴别甲烷与乙烯,又可除去甲烷中混有乙烯的最佳方法是
| A.通入酸性高锰酸钾溶液中 | B.通入足量溴水中 |
| C.一定条件下通入H2 | D.点燃 |
将纯锌片和纯铜片按右图方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是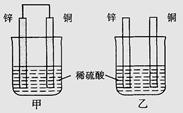
| A.两烧杯中铜片表面均无气泡产生 |
| B.甲中铜片是正极,乙中铜片是负极 |
| C.两烧杯中溶液的pH均增大 |
| D.甲、乙溶液均变蓝 |
在恒容密闭容器中,可逆反应H2(g)+I2(g)  2HI(g) 达到平衡状态时的标志是
2HI(g) 达到平衡状态时的标志是
| A.混合气体的体积恒定不变 |
| B.混合气体的颜色不再改变 |
| C.H2、I2、HI的浓度相等 |
| D.I2在混合气体中的体积分数与H2在混合气体中的体积分数相等 |
A元素的阴离子、B元素的阴离子和C元素的阳离子具有相同的电子层结构。已知A的原子序数大于B的原子序数。则A、B、C三种离子半径大小的顺序是
A. C>B>AB. C>A>B C.A>B>CD. B>A>C