已知某温度下CH3COOH和NH3·H2O的电离常数相等,现向10 mL浓度为0.1 mol·L-1的CH3COOH溶液中滴加相同浓度的氨水,在滴加过程中
| A.水的电离程度先减小再增大 |
B. 始终增大 始终增大 |
| C.n (CH3COOH)与n (CH3COO-)之和始终保持不变 |
| D.当加入氨水的体积为10 mL时,溶液的PH一定为7 |
用0.01mol·L-1 H2SO4和0.01mol·L-1NaOH溶液,中和后加水至100mL。若在滴定时终点有误差:(1)多滴了1滴H2SO4;(2)少滴了1滴H2SO4(1滴为0.05 mL),则(1)和(2)两种情况下c(H+)之比的值是
| A.10 | B.50 | C.5×103 | D.104 |
已知常温下BaSO4(分子量233)的溶解度为2.33×10-4g,则其Ksp为
| A.2.33×10-4 | B.1×10-5 | C.1×10-10 | D.1×10-12 |
MOH和ROH两种一元碱的溶液分别加水稀释时,pH变化如下图所示。下列叙述中不正确的是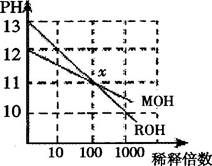
| A.ROH是一种强碱 | B.在x点,MOH并没有完全电离 |
| C.在x点,c(M+)=c(R+) | D.稀释前,c(ROH)=10c(MOH) |
下列各组离子,在所给条件下一定能大量共存的是
| A.pH="0" 的溶液中:Mg2+、Fe3+、NO3-、SO42- |
| B.能和Ca2+生成沉淀的溶液中:Ba2+、K+、CH3COO-、Cl- |
| C.能使碘化钾淀粉试纸变蓝的溶液:Na+、NH4+、S2-、SO32- |
| D.由水电离出的c(OH-)=1×10-13mol/L的溶液中:NH4+、Al3+、NO3-、Cl- |
向ZnSO4溶液中加入Na2S溶液时,得到白色沉淀,然后向白色沉淀上滴加CuSO4溶液,发现沉淀变为黑色,则下列说法不正确的是
| A.白色沉淀为ZnS,而黑色沉淀为CuS |
| B.利用该原理可实现一种沉淀转化为更难溶的沉淀 |
| C.该过程破坏了ZnS的溶解平衡 |
| D.上述现象说明ZnS的Ksp小于CuS的Ksp |