常温下,在10 mL 0.1 mol·L-1 Na2CO3溶液中逐滴加入0.1 mol·L-1 HCl溶液,溶液的pH逐渐降低,此时溶液中含碳微粒的物质的量分数变化如图所示(CO2因逸出未画出,忽略因气体逸出引起的溶液体积变化),下列说法正确的是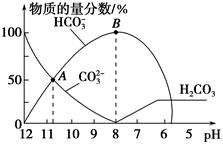
| A.在0.1 mol·L-1 Na2CO3溶液中:c(Na+)+c(H+)=c(CO32-)+c(HCO3-)+c(OH-) |
| B.当溶液的pH为7时,溶液的总体积为20 mL |
| C.在B点所示的溶液中,浓度最大的阳离子是Na+ |
| D.在A点所示的溶液中:c(CO32-)=c(HCO3-)>c(H+)>c(OH-) |
下列说法中不正确的是( )
| A.工业酒精中因含有剧毒物质甲醇而不能用来勾兑饮用酒 |
| B.丁达尔效应能用于区别葡萄糖溶液与淀粉溶液 |
C.2CH3CH2OH CH3CH2OCH2CH3+H2O属于取代反应 CH3CH2OCH2CH3+H2O属于取代反应 |
| D.乙烷在光照条件下与氯气发生取代反应,理论上得到的氯代物最多有4种 |
下列说法中正确的是( )
| A.淀粉和纤维素的分子式均为(C6H10O5)n,它们互为同分异构体 |
| B.乙醇和乙酸都是常用调味品的主要成分 |
| C.聚氯乙烯能使溴的四氯化碳溶液褪色 |
| D.人体不能消化纤维素,所以纤维素在人体中作用不大,人可以不吃富含纤维素的食物 |
下列除去杂质(括号内为杂质)的方法正确的是( )
①乙烷(乙烯) 光照条件下通入Cl2,气液分离
②乙酸乙酯(乙酸) 用饱和碳酸钠溶液洗涤、分液
③苯(乙酸) 用氢氧化钠溶液洗涤、分液
④乙醇(乙酸) 加足量生石灰、蒸馏
| A.①②③ | B.②③④ | C.①③④ | D.①②④ |
如图为实验室制取少量乙酸乙酯的装置图。下列关于该实验的叙述中不正确的是( )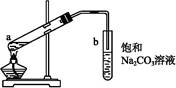
| A.向a试管中先加入浓硫酸,然后边摇动试管边慢慢加入乙醇和冰醋酸 |
| B.试管b中导气管下端管口不能插入液面以下的目的是防止实验过程中产生倒吸现象 |
| C.实验时加热试管a的目的之一是及时将乙酸乙酯蒸出,使平衡向生成乙酸乙酯的方向移动 |
| D.试管b中饱和碳酸钠溶液的作用是吸收随乙酸乙酯蒸出的少量乙酸和乙醇 |
化学已渗透到人类生活的各个方面,下列说法中不正确的是( )
| A.用浸泡过高锰酸钾溶液的硅藻土吸收水果释放的乙烯,可达到水果保鲜的目的 |
B.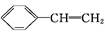 能使酸性KMnO4溶液褪色 能使酸性KMnO4溶液褪色 |
| C.“H7N9”禽流感病毒属于蛋白质,加热会使其变性 |
| D.苯与HNO3的反应和乙烯与Br2的反应属于同一类型的反应 |