硫有多种含氧酸,亚硫酸(H2SO3)、硫酸(H2SO4)、焦硫酸、硫代硫酸(H2S2O3)等等,其中硫酸最为重要,在工业上有广泛的应用,在实验室,浓硫酸是常用的干燥剂。
(1)焦硫酸(H2SO4·SO3)溶于水,其中的SO3都转化为硫酸,若将445g焦硫酸溶于水配成4.00L硫酸,该硫酸的物质的量浓度= mol·L-1;
(2)若以浓硫酸吸水后生成H2SO4·H2O计算,250g质量分数为98%的硫酸能吸收水的质量= 。
铜有两种天然同位素 Cu和
Cu和 Cu,参考铜的原子量(63.5)估算
Cu,参考铜的原子量(63.5)估算 Cu的百分含量约是
Cu的百分含量约是
| A.20% | B.25% | C.50% | D.66.7% E. 75% |
下图是超导化合物----钙钛矿晶体中最小重复单元(晶胞)的结构。请回答: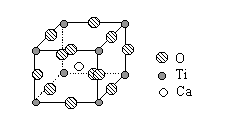
(1)该化合物的化学式为。
(2)在该化合物晶体中,与某个钛离子距离最近且相等的其他钛离子共有个。
(3)设该化合物的式量为M,密度为ag/cm3,阿伏加德罗常数为NA,则晶体中钙离子与钛离子之间的最短距离为。
某课外活动小组将1.100g碳素钢钢样在纯氧中完全燃烧,生成的CO2通入足量NaOH(aq)中,NaOH(aq)增重0.013g。求此钢样中碳的质量分数,并判断这种钢是何种钢。