下列表示对应化学反应的离子方程式正确的是
| A.向FeCl3溶液中加入Mg(OH)2: 3Mg(OH)2+2Fe3+ ="=" 2Fe(OH)3 +3 Mg2+ |
B.草酸使酸性KMnO4溶液褪色: |
C.往NaHS04溶液中滴加Ba(OH)2至溶液呈中性: |
| D.向NaCl0溶液中通人少量的CO2:CO2 +2C1O-+H2O ="=" CO32-+ 2 HC1O已知Ka1(H2 CO3)>Ka( HC1O)>Ka2(H2 CO3) |
已知向品红溶液中加入稀硫酸,溶液颜色加深。现将SO2缓慢通入稀品红溶液中,观察到的现象是()
| A.红色先加深后褪至无色 | B.红色立刻褪去,溶液变为无色 |
| C.红色加深,颜色不褪 | D.红色既不加深也不褪去 |
向某溶液中加入BaCl2溶液,再加入稀硝酸,产生的白色沉淀不消失,下列叙述正确的是()
A.溶液中一定含有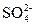 |
| B.溶液中一定含有Ag+ |
C.溶液中一定含有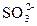 |
D.溶液中可能含有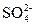 、 、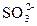 、Ag+中的某一种、两种或三种 、Ag+中的某一种、两种或三种 |
只存在于溶液中的酸是()
| A.HCl | B.H2SO3 | C.H2SO4 | D.H3PO4 |
BaCl2有剧毒,致死量为0.8g,万一不慎误服,应大量吞服鸡蛋清来解毒,并加服一定量药剂,此药剂的主要成分是()
| A.AgNO3 | B.Na2SO4 | C.Na2CO3 | D.MgCl2 |
BaSO4在医学上用作钡餐的理由,其中正确的是()
①既不溶于水又不溶于酸②对人体无害③不易被X射线透过④有治疗疾病的作用
| A.只有① | B.①和③ | C.①和④ | D.②和③ |