【选修5—有机化学基础】
有机物A〜M有如图所示转化关系,A与F分子中所含碳原子数相同,且均能与 NaHCO3溶液反应;F的分子式为C9H10O2,且不能使溴的CCl4溶液褪色;D能发生银镜反应;M.与NaOH溶液反应后的产物,其一氯代物只有一种。
请回答:
(1)B、F的结构简式分别为____________、____________
(2)反应①〜⑦中,属于消去反应的是________(填反应序号)。
(3)D发生银镜反应的化学方程式为_______________________;反应⑦的化学方程式为________________________
(4)A的相对分子质量在180〜260之间,从以上转化中不能确认A中的某一官能团,确 定该官能团的实验步骤和现象为________________________________________
(5)符合下列条件的F的同分异构体共有________种。
a.能发生银镜反应
b.能与FeCl3溶液发生显色反应
c.核磁共振氢谱上有四个峰,其峰面积之比为1:1:2:6
在一定温度下,把2体积N2和6体积H2通入一个带活塞的体积可变的容器中,活塞的一端与大气相通(如上图)。
容器中发生以下反应:N2+3H2 2NH3(正反应放热),若反应达到平衡后,测得混合气体为7体积。据此回答下列问题:
2NH3(正反应放热),若反应达到平衡后,测得混合气体为7体积。据此回答下列问题:
(1)保持上述温度不变,设a、b、c分别代表初始加入的N2、H2和NH3的体积,如果反应达到平衡后混合气体中各物质的体积分数仍与上述平衡时完全相同。那么:①若a=1,c=2,则b=_________,在此情况下,反应起始时将向_____________(填“正”或“逆”)方向进行。
②若需规定起始时,反应向逆方向进行,则c的范围是___________。
(2)在上述装置中,若需控制平衡后混合气体为6.5体积,则可采取的措施是_________,原因是______________________________。
在一固定容积的密闭容器中,在一定条件下进行以下化学反应:A(g)+2B(g) 3C(g)。已知加入1 mol A和3 mol B,且达到化学平衡后,生成了a mol C。
3C(g)。已知加入1 mol A和3 mol B,且达到化学平衡后,生成了a mol C。
(1)达到化学平衡时,C在反应混合气中物质的量百分含量为_________(用字母a表示)。
(2)在相同实验条件下,若在同一容器中改为加入2 mol A和6 mol B,达到化学平衡后,C的物质的量为________mol(用字母a表示)。此时C在反应混合气体中的物质的量的百分含量_________(填“增大”“减小”或“不变”)。
(3)在相同实验条件下,若在同一容器中改为加入2 mol A和8 mol B,并要求达到化学平衡后C在反应混合气体中的百分含量不变,则还应加入C_________mol。
在容积可变的密闭容器中,可逆反应2HI(g) H2(g)+I2(g)已达平衡,若将体积缩小,在缩小的过程中:
H2(g)+I2(g)已达平衡,若将体积缩小,在缩小的过程中:
(1)正反应速率______________;
(2)逆反应速率______________;
(3)平衡______________;
(4)容器内颜色______________;
(5)H2的质量分数______________;
(6)混合气体的平均相对分子质量______________;
(7)H2的浓度______________;
(8)HI的分解率______________;
(9)混合气体的密度______________;
(10)混合气体的质量______________。(用“变大”“变小”“不变”“加深”“变浅”填写)
X、Y、Z三种物质有如图所示转化关系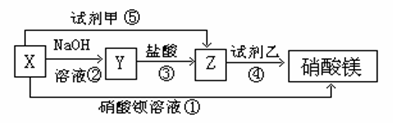
(1)根据上述转化关系,写出下列物质的化学式:X、Y、
Z试剂甲,试剂乙(每空1分)。
(2)写出上述各步反应①~⑤的离子方程式:
①;②;
③;④ ;
⑤(每空2分)。
现有四瓶溶液,分别是H2SO4、BaCl2、Na2SO4、Na2CO3中的一种,根据以下实验,请分别确认A、B、C、D各是什么物质?
A加入B中无反应。A加入C中有气体产生,D加入A中有沉淀产生。
则:A:________; B:________;C:_________;D:___________(每空1分)。
写出A与C反应的离子方程式
A与D反应的离子方程式。_______________(每空2分)。