钙元素是人体必需的常量元素,所有的细胞都需要钙元素。正常人体血液含Ca2+为2.2×10-3 ~2.7×10-3mol·L-1。现抽取某人血样10ml。稀释后用草酸铵[(NH4)2C2O4]溶液处理,使Ca2+完全转变为草酸钙CaC2O4沉淀;过滤,洗涤,将得到的沉淀用稀硫酸溶解可得到草酸(H2C2O4),并用2.0ml 5.0×10-3 mol·L-1KMnO4溶液与溶解得到的草酸恰好完全反应。据此可以求此人血液中的Ca2+的浓度,并判断其血液含钙量是否正常。(提示2KMnO4+5H2C2O4+3H2SO4=2MnSO4+K2SO4+10CO2+8H2O)
(1)配制5.0×10-3 mol·L-1KMnO4 200mL溶液,需要称取KMnO4固体的质量是 g;
(2)每消耗草酸0.5mol,转移电子的物质的量为 mol;
(3)此人血液中的Ca2+的浓度为 mol·L-1。
某有机物只含碳、氢、氧三种元素,其质量比为6:1:8。该有机物蒸气的密度是相同条件下乙烷的2倍,试求该有机物的相对分子质量及分子式。根据下列条件写出该有机物的同分异构体的结构简式:
①该有机物常温下能跟碳酸氢钠溶液反应;
②该有机物能产生银镜;
③该有机物既能产生银镜,又能与钠反应生成氢气
由A、B两种物质组成的混合气体,其平均相对分子质量随A的物质的量分数变化关系如右图所示。
求:A、B的相对分子质量,若测得混合气体中仅含两种元素,A、B都是有机物时,写出化学式。
在100mL 2.00mol/L的Ba(OH)2溶液中滴加100mL NaHSO4溶液,测得溶液的pH为1.00,求产生的沉淀的质量,以及NaHSO4溶液的物质的量浓度(设两种溶液混合时体积变化忽略不计)。
将2.56g金属铜投入到一定物质的量浓度的浓硝酸中,生成气体颜色越来越浅,当恰好完全反应时,共收集到标准状况下896mL气体。
(1)、写出可能发生反应的化学方程式
____________________________________________________________
_____________________________________________________________
(2)、计算参加反应的硝酸的物质的量是多少?
(3)将盛有生成气体的容器倒扣在水槽中,通入标准状况下一定体积的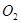 ,恰好使气体完全溶于水。则通入
,恰好使气体完全溶于水。则通入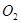 的体积为多少?(3分)
的体积为多少?(3分)
物质的量相同的NaHCO3和KHCO3固体混合物9.20g与100mL盐酸反应。
(1)欲求标准状况下生成CO2的体积,还需要什么数据__________________。(讨论(2)的问题中,该数据用a表示)
(2)讨论a值的变化时,产生CO2的体积(标准状况)
| a |
生成CO2的体积(L) |