25°C时,c(CH3COOH)+c(CH3COO-)=0.1 mol/L的醋酸、醋酸钠混合溶液中,c(CH3COOH)、
c(CH3COO-)与pH的关系如图所示。下列有关该溶液的叙述不正确的是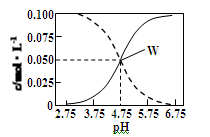
| A.pH=5的溶液中:c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-) |
| B.溶液中:c(H+)+c(Na+)=c(CH3COO-)+c(OH-) |
| C.由W点可以求出25°C时CH3COOH的电离常数 |
| D.pH =4的溶液中:c(H+)+c(Na+)+c(CH3COOH)-c(OH-)=0.1 mol/L |
下列操作中,溶液的颜色不发生变化的是( )
| A.NaHCO3溶液中滴加盐酸 |
| B.Fe2(SO4)3溶液中滴加KSCN溶液 |
| C.FeCl2溶液中滴加氯水 |
| D.FeCl3溶液中加入还原铁粉 |
实验室中,要使AlCl3溶液中的Al3+全部沉淀出来,适宜用的试剂是( )
| A.NaOH溶液 | B.盐酸 |
| C.氨水 | D.Ba(OH)2溶液 |
要除去Fe2O3中混有的Al2O3,最好的方法是( )
| A.用盐酸洗涤过滤 | B.加热用H2还原 |
| C.加热用CO还原 | D.用NaOH洗涤、过滤 |
要除去CO2中混有的少量HCl气体,最好的方法是将气体通过( )
| A.饱和NaHCO3溶液 | B.Na2CO3溶液 |
| C.饱和石灰水 | D.烧碱溶液 |
现有一块铝铁合金,欲测定其铝的质量分数,切下W g合金,溶于盐酸中,再加入过量NaOH溶液,滤出沉淀,将沉淀在空气中充分灼烧,最后得到W g红棕色粉末。则此合金中铝的质量分数约为( )
| A.20% | B.30% | C.70% | D.80% |