下列离子方程式书写不正确的是
| A.盐酸与Na2SiO3溶液混合:SiO32-+2H+===H2SiO3↓ |
| B.往澄清石灰水中通入过量SO2:SO2+Ca2++2OH-===CaSO3↓+H2O |
| C.NO2通入水中:H2O+3NO2===2H++2NO3-+NO |
D.浓盐酸和二氧化锰共热制取Cl2:MnO2+4H++2Cl-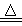 Mn2++Cl2↑+2H2O Mn2++Cl2↑+2H2O |
往碳酸钠稀溶液中加入或通入少量下列物质能反应,但看不到明显现象的是 ( )
| A.Ca(OH)2溶液 | B.Na2O2固体 | C.HCl溶液 | D.CO2 |
下列鉴别纯碱(碳酸钠)和氯化钠的方法中,不可行的是
| A.取少量固体分别滴入稀盐酸 |
| B.取少量固体分别放入水中,观察是否溶解 |
| C.取少量固体分别放入水中,再分别滴入澄清石灰水,观察现象 |
| D.取少量固体分别放入水中,再分别滴入氯化钡溶液 |
下列有关Na2CO3和NaHCO3的说法中正确的是 ( )
| A.两者在医疗上均可用于治疗胃酸过多 |
| B.它们都易溶于水 |
| C.在通常状况下,受热都易分解 |
| D.都可以和NaOH溶液反应 |
欲除去Na2CO3固体中的NaHCO3杂质,可采取的方法是( )
| A.加水溶解后过滤 |
| B.配成溶液后通入足量的CO2气体 |
| C.将固体加热 |
| D.先加足量盐酸后过滤 |
取ag某物质在氧气中完全燃烧,某产物跟过量的Na2O2固体完全反应,反应后固体的质量恰好也增加了ag。下列物质中不能满足上述结果的是(提示:C6H12O6、C2H6O完全燃烧产物都为CO2、H2O) ( )
| A.H2 | B.CO | C.C6H12O6 | D.C2H6O |