下列实验装置图所示的实验操作,不能达到相应实验目的的是
下列实验合理的是
 |
 |
 |
 |
| A.配制一定浓度硫酸 |
B.制备少量氨气 |
C.制备并收集少量NO2气体 |
D.制备少量氧气 |
将足量SO2通入下列各溶液中,所含离子还能大量共存的是
| A.H+、Br -、Fe2+、SO42— | B.NH4+、CO32—、NO3—、SiO32— |
| C.Na+、S2—、OH—、AlO2— | D.Fe3+、Cl-、Ba2+、Al3+ |
下列有关物质分类或归类正确的是
①混合物:盐酸、氯水、水银②化合物:CaCl2、NaOH、HD
③电解质:胆矾、冰醋酸、氧化铝④同素异形体:C60、金刚石、石墨
⑤放热反应:盐酸与氢氧化钠、碳与二氧化碳高温化合成一氧化碳、甲烷燃烧
| A.①③ | B.③④ | C.②③ | D.④⑤ |
化学与生产、生活、社会密切相关,下列有关说法不正确的是
| A.多用电子邮件、MSN、QQ等即时通讯工具,少用传真打印机属于“低碳生活”方式 |
| B.我国神九三位宇航员所穿航天服主要成分是由碳化硅、陶瓷和碳纤维复合而成的,它是一种新型无机非金属材料 |
| C.棉花、蚕丝和人造丝的主要成分都是纤维素 |
| D.日本福岛核电站爆炸时释放的2种放射性同位素131I与137Cs的中子数不等 |
常温下,在 溶液中逐滴加入
溶液中逐滴加入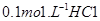 溶液20mL, 溶液的pH逐渐降低,此时溶液中含碳微粒的物质的量分数(ω)变化如右图所示(CO2因逸出未画出),下列说法正确的是
溶液20mL, 溶液的pH逐渐降低,此时溶液中含碳微粒的物质的量分数(ω)变化如右图所示(CO2因逸出未画出),下列说法正确的是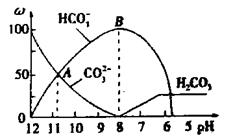
A.在0.1mo1/L Na2CO3溶液中: |
| B.当溶液pH为7时,溶液的总体积为20mL |
| C.在B点所示的溶液中,阳离子浓度最大的是Na |
D.在 A点所示的溶液中: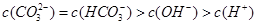 |