用NA表示阿伏加德罗常数的值,下列说法中正确的是
| A.1 mol N2所含有的原子数为NA |
| B.1 mol·L-1 NaCl溶液中含有的钠离子数目为NA |
| C.标准状况下,22.4 LCO所含的原子数为NA |
| D.24 g O2和24 g O3所含的氧原子数都是1.5NA |
下列说法在一定条件下可以实现的是
①酸性氧化物与碱发生反应
②弱酸与盐溶液反应可以生成强酸
③没有水生成,也没有沉淀和气体生成的复分解反应
④两种酸溶液充分反应后的溶液体系为中性
⑤有单质参加的非氧化还原反应
⑥两种氧化物反应的产物有气体
| A.①②③④⑤⑥ | B.②④⑤⑥ | C.①②③⑤ | D.③④⑤⑥ |
下列各种情况下,常温下溶液中一定能大量存在的离子组是
| A.酸性溶液中可能大量存在 : Na+、ClO﹣、SO42﹣、CN﹣ |
| B.无色溶液中可能大量存在 : Al3+、NH4+、Cl﹣、S2﹣ |
| C.pH=7的中性溶液中:Fe3+、K+、Cl-、SO42- |
| D.由水电离出的c(H+)=l×10-12mol/L的溶液中:K+、Ba2+、Cl-、NO3- |
下列制备和收集气体的实验装置合理的是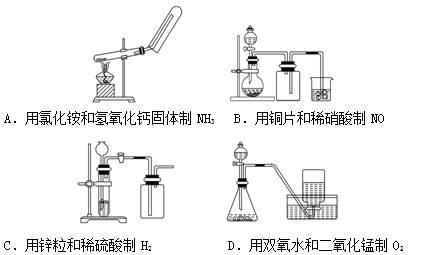
在Al2(SO4)3、K2SO4和明矾的混合溶液中,如果c(SO42-)等于0.2 mol·L-1,当加入等体积的0.2 mol·L-1的KOH溶液时,生成的沉淀恰好溶解,则原混合溶液中K+的物质的量浓度为
| A.0.25 mol·L-1 | B.0.2 mol·L-1 |
| C.0.45 mol·L-1 | D.0.225 mol·L-1 |
下列关于Na2CO3和NaHCO3性质的说法错误的是
| A.热稳定性:NaHCO3<Na2CO3 |
| B.与同浓度盐酸反应的剧烈程度:NaHCO3<Na2CO3 |
| C.相同温度时,在水中的溶解性:NaHCO3<Na2CO3 |
| D.等物质的量浓度溶液的pH:NaHCO3<Na2CO3 |