下列叙述正确的是
| A.光导纤维中所用材料为晶体硅 |
| B.SiO2是酸性氧化物, 所以不与任何酸反应 |
| C.可用Na2SiO3溶液和CO2反应来制备H2SiO3 |
| D.NaOH溶液可以盛装在带玻璃塞的磨口试剂瓶中 |
下列物质能促进水的电离的是
| A.小苏打 | B.醋酸 | C.乙醇 | D.氯化钠 |
镍氢电池的化学方程式为NiO(OH)+MH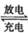 Nio+M+H2O(M为储氢合金,电解质
Nio+M+H2O(M为储氢合金,电解质
为KOH),下列说法不正确的是
| A.充电过程中,电池的负极上发生的反应为H2O +M+ e- =MH+OH- |
| B.储氢合金位于电池的负极 |
| C.放电时,OH-离子向电池的负极移动 |
| D.充电过程中,化学能转化为电能储存在电池中 |
已知反应:2SO2(g)+ O2(g)  2SO3(g)△H<0.某温度下,将2mol SO2和1mol O2置
2SO3(g)△H<0.某温度下,将2mol SO2和1mol O2置
于10L密闭容器中,反应达平衡后,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所
示。则下列说法正确的是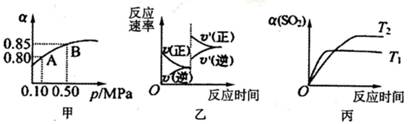
| A.由图甲推断,B点SO2的平衡浓度为0.3mol·L-1 |
| B.由图甲推断,A点对应温度下的平衡常数为80 |
| C.达平衡后,缩小容器容积,则反应速率变化图像可以用图乙表示 |
| D.压强为0.50 MPa时不同温度下SO2转化率与温度关系如丙图,则T2>Tl |
25℃时,0.1mol·L-1CH3COONa溶液pH=a,则
| A.该温度下,CH3COOH的Ka=1014-2a |
| B.该温度下,上述溶液中水的电离度α=(1.8×l0 a -14)% |
| C.升高温度,溶液中c(H+)增大,水解平衡常数K也增大 |
| D.加水稀释,CH3COONa水解程度增大,C(OH-)增大 |
下图是一种综合处理SO2废气的工艺流程。下列说法正确的是
| A.向B溶液中滴加KSCN溶液,溶液变为血红色 |
| B.溶液B转化为溶液C发生的变化的离子方程式为4H++2Fe2++O2=2Fe3++2H2O |
| C.溶液酸性A>B>C |
| D.加氧化亚铁可以使溶液C转化为溶液A |