图1是实验室制取气体的常用装置.
(1)实验室常用过氧化氢溶液和二氧化锰制取氧气,若要控制反应速率,应选择的发生装置是 (填字母,下同);若要收集较为纯净的氧气,应选择的收集装置是 ;
写出该反应的化学方程式 .
(2)实验室用大理石和稀盐酸反应制取二氧化碳,写出该反应的化学方程式 ;若用图2装置检验二氧化碳,气体应从 (填“a”或“b”)端通入,写出发生反应的化学方程式 ;
(3)碱式碳酸铜是一种绿色粉末,受热条件下会分解成三种氧化物,若用实验证明加热碱式碳酸铜有新物质生成,应将干燥的碱式碳酸铜放入 装置进行反应,观察到 ,证明生成物之一为水.
下图甲是A、B、C三种固体物质的溶解度曲线图。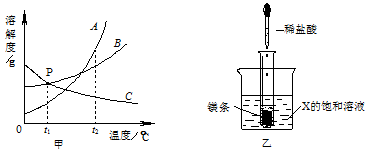
(1)甲图中,t2℃时,A、B、C三种物质中,溶解度最大的是 P点所表示的含义为_____ __ 。
(2)t2℃时,将B物质的不饱和溶液转变成饱和溶液可采取的方法__________________。
(3)如乙图所示,20℃时,把试管放入盛有X的饱和溶液的烧杯中,在试管中加入几小段镁条,再加入5mL稀盐酸,立即产生大量的气泡,同时烧杯中出现浑浊,则X可能为A、B、C三种固体物质中的哪一种? 。
小强设计了一个有趣的实验(如右图所示),经过很长一段时间后,他观察到小试管内有晶体析出。
(1)下面是小强对这种现象解释的部分内容,请你帮他把其余的解释内容续写完整: 浓硫酸具有吸水性,。
(2)若实验前后温度不变,则实验后的硝酸钾溶液的溶质质量分数 (填“大于”、“等于”或“小于”)原饱和硝酸钾溶液的溶质质量分数。
(3)硝酸钾溶液中存在的溶质微粒有 (用符号表示)
【2015年湖北省孝感市】2015年4月25日尼泊尔首都加德满都发生了8.1级大地震,造成大量的人员伤亡和财产损失。中国政府及时派出救援队前往,并为尼泊尔灾区提供了大量的消毒液、大米和帐篷。其中“84”消毒液可用于灾区防疫,其主要成分是次氯酸钠(NaClO),制取它的化学方程式为2NaOH+X===NaClO+NaCl+H2O,则X的化学式为 ,NaClO中氯元素的化合价为 。大米中含有的主要成分为 。帐篷的主要成分聚氯乙烯塑料属于 材料。
【2015年湖南省娄底市】眼镜是人们常用的护眼工具,下图是一款变色眼镜的示意图: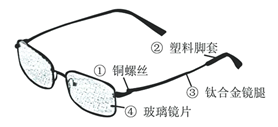
回答下列问题:
(1)图中所标物质属于有机合成材料的是 (填序号)
(2)该款变色眼镜的玻璃里加入了溴化银(AgBr)和氧化铜。在强光照射下,溴化银分解成单质溴(Br2)和银,玻璃颜色变深,该反应的化学方程式为 ;当光线变暗时,溴和银在氧化铜作用下,又立即化合成溴化银,玻璃颜色变浅。氧化铜在该反应中起 作用。
【2015年江苏省南京市】物质之间存在联系,找出联系、发现规律是我们学好化学的一种基本方法。
(1)请你仿照下表中的示例,找出CO2、CH4、C2H2(乙炔)、C2H4(乙烯)这四种气体之间存在的另外两个规律并排序。
| 规律 |
排序 |
| 示例:标准状况下,密度由大到小 |
CO2、C2H4(乙烯)、C2H2(乙炔)、CH4 |
(2)某气体由CH4、C2H2、C2H4中的一种或几种组成,取该气体样品在氧气中完全燃烧,测得生成的二氧化碳和水的质量比为22:9。下列对该气体组成判断正确的是_______________。
A.该气体中一定含有C2H4 B.该气体中一定没有CH4
C.该气体中可能含有C2H2 D.该气体不可能同时含有CH4、C2H2、C2H4