现有乙酸、乙烯和丙烯(C3H6)的混合物,其中氧的质量分数为a,则碳的质量分数是()
A.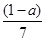 |
B.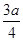 |
C.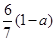 |
D.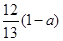 |
利用某些有机物之间的相互转换可以贮存太阳能,如原降冰片二烯(NBD)经过太阳光照转化成为四环烷(Q)的反应为如右图所示,以下叙述不正确的是()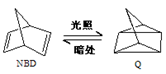
A.NBD的能量比Q的能量低
B.NBD和Q互为同分异构体
C.NBD能发生加成反应而Q不能
D.NBD不能使酸性KMnO4溶液褪色而Q能
25℃、101 kPa下,碳、氢气、甲烷和葡萄糖的燃烧热依次是393.5 kJ/mol、285.8 kJ/mol、890.3 kJ/mol、2800 kJ/mol,则下列热化学方程式正确的是
| A.C(s)+1/2O2(g)=CO(g) △H =" -" 393.5 kJ/mol |
| B.2H2(g)+O2(g)=2H2O(l) △H =" +" 571.6 kJ/mol |
| C.CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H =" -" 890.3 kJ/mol |
| D.C6H12O6(s) +6O2(g)=6CO2(g)+6H2O(l) △H =" -" 2800 kJ/mol |
甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
①CH3OH(g)+H2O(g)===CO2(g)+3H2(g) ΔH =+49.0 kJ/mol
②CH3OH(g)+1/2O2(g)===CO2(g)+2H2(g) ΔH =-192.9 kJ/mol
下列说法正确的是( )
| A.CH3OH的燃烧热为192.9 kJ/mol |
B.反应①中的能量变化如图所示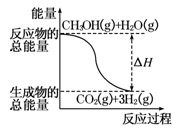 |
| C.CH3OH转变成H2的过程一定要吸收能量 |
| D.根据②推知反应:CH3OH(l)+1/2O2(g)===CO2(g)+2H2(g)的ΔH>-192.9 kJ/mol |
5月3日,广东省发现部分患者使用了齐齐哈尔第二制药有限公司生产的“亮菌甲素注射液”后,出现了严重不良反应,并有多人死亡。目前这起假药案的成因已经水落石出:该公司采购人员在购买药用辅料丙二醇(结构简式为HOCH2CH2CH2OH)时,为图便宜,购入了假冒丙二醇的二甘醇(结构简式为HOCH2CH2—O—CH2CH2OH)并作为辅料用于“亮菌甲素注射液”的生产,从而酿成多人死伤的惨剧。关于丙二醇与二甘醇的说法中正确的是( )。
| A.丙二醇与二甘醇互为同系物 |
| B.丙二醇和二甘醇都互为同分异构体 |
| C.1 mol丙二醇与二甘醇的混合物可以与足量金属钠反应生成11.2 L氢气 |
| D.丙二醇与二甘醇都能发生取代反应 |