下列反应中,水作还原剂的是
| A.2Na+2H2O=2NaOH+H2↑ | B.Cl2+H2O=HCl+HClO |
| C.2F2+2H2O=4HF+O2 | D.SO2+H2O=H2SO3 |
加碘食盐中含有碘酸钾(KIO3),现以电解法制备碘酸钾,实验装置如图所示。先将一定量的碘溶于过量氢氧化钾溶液,发生反应:3I2+6KOH=5KI+KIO3+3H2O,将该溶液加入阳极区,另将氢氧化钾溶液加入阴极区,开始电解。下列说法正确的是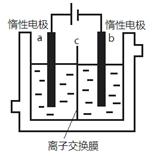
| A.a电极是阴极 |
| B.a极区的KI最终转变为KIO3 |
C.阳极电极反应:4OH--4e-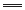 2H2O+O2↑ 2H2O+O2↑ |
| D.电解过程中OH—从a极区通过离子交换膜c进入b极区 |
下列说法正确的是
| A.常温下能够进行的化学反应都是放热反应,高温下进行的反应都是吸热反应 |
| B.常温常压下,pH = 1的盐酸中约含有6.02×1023个氢离子 |
| C.常温常压下,0.5mol氮气和氢气的混合气体体积大于11.2L |
| D.原电池装置的正、负极可以是同一种金属 |
将浓度为18.4mol/L质量分数为98%的浓硫酸加水稀释至9.2 mol/L,则稀释后溶质的质量分数为
A大于49% B 小于 49 % C 等于49% D 无法确定
标况下,电解一定物质的量浓度的CuSO4溶液一段时间后,加入0.2molCu(OH)2固体使溶液完全恢复到初始状态,则此过程中共产生气体
| A. 6.72L | B. 8.96L | C.11.2L | D.5.6L |
已知NA表示阿伏加德罗常数的值,下列叙述正确的是
| A.1mol苯乙烯中含有的碳碳双键数为4NA |
| B.6.2g氧化钠晶体中含有0.2NA个Na+ |
| C.标准状况下,22.4L空气含有NA个单质分子 |
| D.1 mol/L NH4Cl溶液中,NH4+的数目小于NA |