用物质的量都是0.1mol的HCN和NaCN混合后配成1L溶液,已知溶液中的c(CN-)<c(Na+),下列关系式正确的是
| A.c(H+)<c(OH-) | B.c(HCN)<c(CN-) |
| C.c(CN-)+c(OH-) = 0.1mol・L-1 | D.c(HCN)+c(CN-) = 0.2mol・L—1 |
用惰性电极电解一定浓度的硫酸铜溶液,通电一定时间后,向所得溶液中加入0.1molCu2(OH)2CO3后恰好恢复到电解前的浓度和pH(不考虑二氧化碳的溶解)。则电解过程中共转移电子数为
| A.0.4mol | B.0.5mol | C.0.6mol | D.0.8mol |
LiFePO4电池具有稳定性高、安全、对环境友好等优点,可用于电动汽车。电池反应为:FePO4+Li放电充电LiFePO4,电池的正极材料是LiFePO4,负极材料是石墨,含Li+导电固体为电解质。下列有关LiFePO4电池说法正确的是
| A.可加入硫酸以提高电解质的导电性 |
| B.充电过程中,电池正极材料的质量减少 |
| C.放电时电池内部Li+向负极移动 |
| D.放电时电池正极反应为:FePO4+Li++e-=LiFePO4 |
下列说法或表示方法正确的是
| A.等质量的硫蒸气和硫固体分别完全燃烧生成等量二氧化硫时放出的热量相同 |
| B.由C(金刚石,s)=C(石墨,s)△H=-1.90 kJ·mol-1,可知石墨比金刚石稳定 |
| C.氢气的燃烧及氢气还原氧化铜的反应都是放热反应 |
| D.1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热 |
某小组为研究电化学原理,设计如图装置。下列叙述不正确的是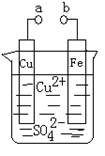
| A.a和b不连接时,铁片上发生的反应为:Cu2++Fe= Cu+Fe2+ |
| B.a和b用导线连接时, Cu2+向铁电极移动 |
| C.a和b分别连接直流电源正、负极,铜片会溶解 |
| D.无论a和b是否连接,铁片均会溶解,溶液从蓝色逐渐变成浅绿色 |
下列叙述中,不能用平衡移动原理解释的是
| A.红棕色的NO2,加压后颜色先变深后变浅 |
| B.高压比常压有利于合成NH3的反应 |
| C.由H2(g)、I2(g)、HI(g)气体组成的平衡体系加压后颜色变深 |
| D.黄绿色的氯水光照后颜色变浅 |