下列说法正确的是()
| A.光导纤维的主要成份是硅 |
| B.常用氢氟酸(HF)来刻蚀玻璃 |
| C.制普通玻璃的主要原料是烧碱、石灰石、石英 |
| D.实验室用带玻璃塞的试剂瓶保存氢氧化钠溶液 |
下列关于催化剂的说法不正确的是()
| A.温度越高,催化剂的催化效果越好 |
| B.汽车排气管上的“催化转化器”能减少有害气体排放 |
| C.催化剂可以改变化学反应速率,但厦应前后质量和化学性质不变 |
| D.锌与盐酸反应时,加入几滴硫酸铜溶液可加快反应速率,但硫酸铜不作催化剂 |
下列化学用语正确的是()
A.硫的原子结构示意图: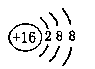 |
B.顺-2-丁烯的结构简式: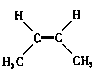 |
| C.乙酸的实验式:C2H4O2 |
| D.原子核内有8个中子的氧原子:188O |
下列说法正确的是()
| A.填埋法是垃圾处理的最佳方法 |
| B.酸雨形成的主要原因是汽车尾气的任意排放 |
| C.维生素C受热更易被氧化,故有些新鲜蔬菜生吃较好 |
| D.淀粉、纤维素,、蛋白质和油脂均属于天然高分子化合物 |
常温下,用0.1000 mol/L NaOH溶液滴定20. 00 mL 0.1000 mol/L HCl溶液,滴定曲线,如下图所示。下列说法不正确的是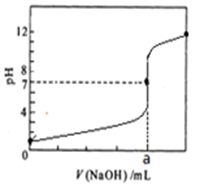
| A.a = 20.00 |
| B.滴定过程中,可能存在:c(Cl-)>c(H+)>c(Na+)>c(OH-) |
| C.若用酚酞作指示剂,当滴定到溶液明显由无色变为红色时停止滴定 |
| D.若将盐酸换成同浓度的醋酸,则滴定到pH=7时,a>20.00 |