关于胶体和溶液的区别,下列叙述中正确的是
| A.溶液呈电中性,胶体带有电荷 |
| B.溶液中溶质粒子能通过滤纸,胶体中分散质粒子不能通过滤纸 |
| C.溶液中通过一束光线没有特殊现象,胶体中通过一束光线出现明显光带 |
| D.溶液稳定,放置后不会生成沉淀;胶体不稳定,放置会生成沉淀 |
常温下,下列说法正确的是
| A.C(石墨,s) = C(金刚石,s);DH>0,所以石墨比金刚石稳定 |
| B.使紫色石蕊试液变红的溶液中Fe2+、Mg2+、NO3-、Cl-一定能够大量共存 |
| C.明矾和漂白粉常用于自来水的净化和杀菌消毒,两者的作用原理相同 |
D.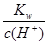 =0.1mol/L的溶液中Na+、K+、SiO32-、NO3-一定不能大量共存 =0.1mol/L的溶液中Na+、K+、SiO32-、NO3-一定不能大量共存 |
设NA表示阿伏加德罗常数的值,下列叙述错误的是
A.在18g 中含有 中含有 个氧原子 个氧原子 |
| B.在反应KIO3+6HI =KI +3I2+3H2O中,每生成3 mol I2转移的电子数为6 NA |
| C.常温常压下,Na2O2与足量H2O反应,共生成0.2molO2,转移电子的数目为0.4NA |
| D.25℃,1L pH=13的NaOH溶液中含有OH-的数目为0.1NA |
下列说法错误的是
| A.K2FeO4能与水作用生成Fe(OH)3胶体和O2,可用于净化自来水并杀菌消毒 |
| B.分散质粒子的直径:Fe(OH)3悬浊液>Fe(OH)3胶体>FeCl3溶液 |
| C.若要除去CO2中含有的少量SO2气体,可通过盛有饱和NaHCO3溶液的洗气瓶 |
| D.对“地沟油’’蒸馏可以获得汽油 |
在温度T1和T2时,分别将0.50 mol CH4和1.2mol NO2充入1 L的密闭容器中发生反应:CH4(g)+2NO2(g)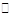 N2(g)+CO2(g)+2H2O(g)△H=akJ/mol。测得有关数据如下表:
N2(g)+CO2(g)+2H2O(g)△H=akJ/mol。测得有关数据如下表:
| 温度 |
时间/min 物质的量 |
0 |
10 |
20 |
40 |
50 |
| T1 |
n(CH4)/mol |
0.50 |
0.35 |
0.25 |
0.10 |
0.10 |
| T2 |
n(CH4)/mol |
0.50 |
0.30 |
0.18 |
x |
0.15 |
下列说法正确的是
A.T1>T2,且a>0
B.当温度为T2、反应进行到40 min时, x>0.15
C.温度为T2时,若向平衡后的容器中再充入0.50 mol CH4和1.2mol NO2,重新达到平衡时,n(N2)=0.70mol
D.温度为T1时,若起始时向容器中充入0.50 mol CH4(g)、0.50 molNO2(g)、1.0 mol N2(g)、2.0 molCO2(g)、0.50 molH2O(g),反应开始时,ν(正)>ν(逆)
25℃时,向20 mL 0.2 mol/L H2A(某二元弱酸)溶液中滴加0.2 mol/L NaOH溶液,有关微粒的物质的量变化如下图(其中I代表H2A,II代表HA-,III代表A2-)。根据图示判断,下列说法中正确的是
A.当V(NaOH)=20mL时,所得溶液中:c(OH-)> c(H+)
B.当V(NaOH)=30mL时,所得溶液中:2c(H+) + c(HA-)+ 3c(H2A) = c(A2-) + 2 c(OH-)
C.当V(NaOH)=40mL时,所得溶液中:c(Na+)> c(A2-) >c(H+)> c(HA-) >c(OH-)
D.在NaHA溶液中:c(OH-)+2c(A2-) = c(H+)+2c(H2A)