Ⅰ.近年来,我国储氢碳管研究获得重大进展,电弧法合成碳纳米管,长伴有大量物质——碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯,其反应的化学方程式为:
__C+___K2Cr2O7+__H2SO4(稀)→___CO2↑+__K2SO4+Cr2(SO4)3+__ ___
(1)完成并配平上述反应的化学方程式。
(2)此反应的氧化剂______,还原剂______。
(3)硫酸在上述反应中表现出的性质是____________(填选项编号)。
| A.酸性 | B.氧化性 | C.吸水性 | D.脱水性 |
上述反应若产生11克气体物质,则转移电子的数目___________。
Ⅱ.X元素的原子核外有2个电子层,其中L层有5个电子,该元素在周期表中的位置为________,最高价氧化物的化学式为________,该元素的氢化物和最高价氧化物对应水化物反应的化学方程式为________________________________.
写出下列化学方程式,并注明反应类型
(2)溴乙烷与氢氧化钠的醇溶液在加热条件下反应,反应类型:。
(3)苯酚与溴水的反应,反应类型:。
4分)写出以下键线式所表示的有机物的结构简式: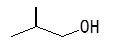
,属于该类有机物的同分异构体还有种。
用质量分数为37.5%的浓盐酸(密度为1.16 g / cm3)配制成1 mol / L的稀盐酸。现实验室仅需要这种盐酸220 mL。试回答下列问题:
(1)配制稀盐酸时,应选用容量为mL的容量瓶;
(2) 经计算需要mL浓盐酸,在量取时宜选用下列量筒中的。
| A.5 mL | B.10 mL | C.25 mL | D.50 mL |
(3) 在量取浓盐酸后,进行了下列操作:
①等稀释的盐酸其温度与室温一致后,沿玻璃棒注入250 mL容量瓶中。
② 往容量瓶中小心加蒸馏水至液面接近环形标线2~3 cm处,改用胶头滴管加蒸馏水,使溶液的凹面底部与瓶颈的环形标线相切。
③ 在盛盐酸的烧杯中注入蒸馏水几十毫升,并用玻璃棒搅动,使其混合均匀。
④ 用蒸馏水洗涤烧杯和玻璃棒2至3次,并将洗涤液全部注入容量瓶。
上述操作中,正确的顺序是(填序号)。
(4) 在上述配制过程中,用刚刚洗涤洁净的量筒来量取浓盐酸,其配制的稀盐酸浓度是
(填“偏高”、“偏低”、“无影响”)。若未用蒸馏水洗涤烧杯内壁或未将洗涤液注入容量瓶,则配制的稀盐酸浓度是(填“偏高”、“偏低”、“无影响”)。
用20g烧碱配制成500mL溶液,其物质的量浓度为mol/L;从中取出1mL,其物质的量浓度为mol/L;含溶质g。若将这1mL溶液用水稀释到100mL,所得溶液中溶质的物质的量浓度为mol/L,其中含Na+g。
阿司匹林(乙酰水杨酸)是由水杨酸和乙酸酐合成的:
在生成乙酰水杨酸的同时,水杨酸分子之间也能发生聚合反应,生成少量聚合物(副产物).合成乙酰水杨酸的实验步骤如下:
①向150 mL 干燥锥形瓶中加入2 g水杨酸、5 mL乙酸酐和5滴浓硫酸,振荡,待其溶解后,控制温度在85~90℃条件下反应5~10 min,然后冷却,即有乙酰水杨酸晶体析出.
②减压过滤,用滤液淋洗锥形瓶,直至所有晶体收集到布氏漏斗中.抽滤时用少量冷水洗涤晶体几次,继续抽滤,尽量将溶剂抽干.然后将粗产品转移至表面皿上,在空气中风干.
③将粗产品置于100 mL 烧杯中,搅拌并缓慢加入25 mL 饱和碳酸氢钠溶液,加完后继续搅拌2~3 min,直到没有二氧化碳气体产生为止.过滤,用5~10 mL 蒸馏水洗涤沉淀.合并滤液于烧杯中,不断搅拌,慢慢加入15 mL 4 mol/L盐酸,将烧杯置于冰水中冷却,即有晶体析出.抽滤,用冷水洗涤晶体1~2次,再抽干水分,即得产品.
(1)第①步中,要控制温度在85~90℃,应采用的________________________,用这种方法加热需要的玻璃仪器有________.
(2)在第②步中,用冷水洗涤晶体,其目的是___________________________________.
(3)在第③步中,加入饱和碳酸氢钠溶液的作用是________,加入盐酸的作用是________.
(4)如何检验产品中是否混有水杨酸?________________________________.