探究浓硫酸和铜的反应,下列装置或操作正确的是
| A.用装置甲进行铜和浓硫酸的反应 |
| B.用装置乙收集二氧化硫并吸收尾气 |
| C.用装置丙稀释反应后的混合液 |
| D.用装置丁测定余酸的浓度 |
“魔棒”常被用于晚会现场气氛的渲染。其发光原理是利用H2O2氧化草酸二酯产生能量,该能量被传递给荧光物质后发出荧光,草酸二酯(CPPO)结构简式如图所示:
下列有关说法不正确的是:()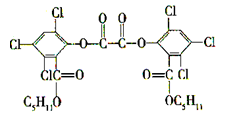
| A.草酸二酯属于芳香族化合物 |
| B.草酸二酯的分子式为C26H23O8Cl6 |
| C.1mol草酸二酯最多可与4molNaOH反应 |
| D.草酸二酯难溶于水 |
有两种饱和一元醇的混合物2.293 g与足量的Na充分反应,生成的氢气在标准状况下的体积为560 mL,这两种醇分子中相差一个碳原子。则这两种醇是( )
| A.甲醇和乙醇 | B.乙醇和丙醇 | C.丙醇和丁醇 | D.无法判断 |
下列实验处理可行的是()
①.将 与NaOH的醇溶液共热制备CH3—CH═CH2
与NaOH的醇溶液共热制备CH3—CH═CH2
②.向甲酸和甲醛的混合物中加入氢氧化钠溶液,中和甲酸后,加入新制的氢氧化铜加热——检验混合物中是否含有甲醛
③.向丙烯醛(CH2=CH—CHO)中滴入KMnO4(H+)溶液,观察紫色褪去,能证明结构中存在碳碳双键
④.实验时手指不小心沾上苯酚,立即用70o以上的热水清洗
| A.只有① | B.只有①④ | C.只有①③④ | D.都不能 |
某一元醛发生银镜反应,可得21. 6g Ag,等量的该醛完全燃烧时,可生成5.4g H2O,则该醛可能是()
A 乙醛(CH3CHO) B 丙烯醛(CH2=CH—CHO)
C 丙醛(CH3CH2CHO) D 丁烯醛(CH2=CHCH2CHO)
下列各组物质中当总质量一定时,不论按何种比例混合,充分燃烧后,生成水的质量为一常量,且生成CO2质量也为一定值的是
| A.甲醛、乙醇、乙二醇 | B.苯、苯酚、苯乙烯 |
| C.甲烷、乙烯、乙烷 | D.甲醛、乙酸、葡萄糖 |