现有甲、乙、丙、丁四种短周期元素,它们之间的关系如下:
Ⅰ.原子半径:甲<丙<乙<丁
Ⅱ.原子的最外层电子数:甲+丙=乙+丁=8
Ⅲ.原子的核外电子层数:丁>乙=丙=2甲
Ⅳ.乙元素的主要化合价:最高正价+最低负价=2
则下列说法不正确的是
| A.乙元素的最外层有5个电子,其氢化物含有极性键 |
| B.四种元素中丙的非金属性最强,其最高价氧化物对应的含氧酸酸性最强 |
| C.丁元素的氧化物对应的水化物与乙元素最高价氧化物对应水化物恰好完全反应形成的盐溶液显酸性 |
| D.乙、丙两元素形成的简单氢化物稳定性丙的强于乙 |
某一密闭绝热容器中盛有饱和Ca(OH)2溶液,当加入少量CaO粉末,下列说法正确的是
①有晶体析出 ②c[Ca(OH)2]增大 ③pH不 变 ④c(H+)·c(OH)-的积不变⑤c(H
变 ④c(H+)·c(OH)-的积不变⑤c(H +)一定增大
+)一定增大
| A.① | B.①⑤ | C.①②④ | D.①③ |
用标准NaOH溶液滴定未知浓度的盐酸,选用酚酞作指示剂,造成测定结果偏高的原因是
| A.配制标准溶液的NaOH中混有Na2CO3杂质 |
| B.盛放未知液的锥形瓶中又加入少许的蒸馏水 |
| C.滴定前读数时仰视,滴定到终点读数时俯视 |
| D.滴定到溶液呈浅红色时立即停止滴定,振荡后又恢复到无色 |
向体积为Va的0.05mol·L-1CH3COOH溶液中加入体积为V b的0.05mol·L-1KOH溶液,下列关系错误的是
b的0.05mol·L-1KOH溶液,下列关系错误的是
| A.Va>Vb时:c(CH3COOH)+c(CH3COO-)>c(K+) |
| B.Va=Vb时:c(CH3COOH)+c(H+)=c(OH-) |
| C.Va<Vb时:c(CH3COO-)>c(K+)>c(OH-)>c(H+) |
| D.Va与Vb任意比时:c(K+)+c(H+)=c(OH-)+c(CH3COO-) |
如图装置中,U型管内为红墨水,a、b试管内分别盛有食盐水和氯化铵溶液,各加入生铁块,放置一段时间。下列有关描述错误的是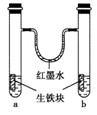
| A.生铁块中的碳是原电池的正极 |
| B.红墨水柱两边的液面变为左低右高 |
C.两试管 中相同的电极反应式是:Fe-2e-→Fe2+ 中相同的电极反应式是:Fe-2e-→Fe2+ |
| D.a试管中发生了吸氧腐蚀,b试管中发生了析氢腐蚀 |
有4种混合溶液,分别由等体积0.1mol/L的2种溶液混合而成:①CH3COONa与HCl;②CH3COONa与NaOH;③CH3COONa与NaCl;④CH3COONa与NaHCO3,下列各项排序正确的是
A.p H:②>③>④>① H:②>③>④>① |
B.c(CH3COO-):②>④>③>① |
| C.溶液中c(H+):①>③>②>④ | D.c(CH3COOH):①>④>③>② |