下列水溶液中能大量共存的一组离子是
| A.K+、Al3+、CO32-、Cl- | B.Na+、H+、SO42-、SiO32- |
| C.H+、Mg2+、SO42- 、I- | D.H+、Fe2+、Cl—、NO3— |
光气(COCl2)的分解反应为:COCl2(g) Cl2(g)+CO(g);△H=+108kJ·mol-1。反应体系中各物质的浓度在不同条件下的变化如图8所示(10~14 min的COCl2浓度变化未标出):
Cl2(g)+CO(g);△H=+108kJ·mol-1。反应体系中各物质的浓度在不同条件下的变化如图8所示(10~14 min的COCl2浓度变化未标出):
下列说法正确的是
| A.COCl2在5~6 min和15~16 min时平均反应速率:v(5~6)< v(15~16) |
| B.第10 min时,改变反应条件,反应重新达到平衡前:v(正)>v(逆) |
| C.第12 min时,反应重新达到平衡,c(COCl2)≈ 0.03 mol·L-1 |
| D.第14 min时,改变的条件是减小压强,随着平衡的移动,COCl2的转化率减小 |
下列有关溶液中微粒浓度关系的叙述正确的是
| A.c(NH4+)相等的(NH4)2SO4、NH4HSO4、NH4Cl溶液中:c(NH4HSO4) > c[(NH4)2SO4]> c(NH4Cl) |
| B.已知HF的酸性比CH3COOH强,pH相等的NaF与CH3COOK溶液中,[c(Na+)-c(F-)]< [c(K+)-c(CH3COO-)] |
| C.等物质的量浓度Na2CO3溶液和NaHCO3溶液等体积混合,所得溶液中:c(CO32-)+2c(OH-)=2c(H+)+c(HCO3-)+3c(H2CO3) |
| D.溶有等物质的量NaClO、NaHCO3的溶液中:c(HClO)+c(C1O-)=c(HCO3-)+c(H2CO3)+c(CO32-) |
空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池。下图为RFC工作原理示意图,有关说法正确的是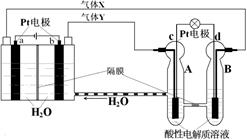
A.转移0.1mol电子时,a电极产生标准状况下O2 1.12L
B.b电极上发生的电极反应是:2H2O+2e-=H2↑+2OH-
C.c电极上进行还原反应,B电池中的H+可以通过隔膜进入A池
D.d电极上发生的电极反应是:O2+4H++4e-=2H2O
下述实验不能达到预期实验目的的是
| 序号 |
实验内容 |
实验目的 |
| A |
室温下,用pH试纸测定浓度为0.1mol·L-1NaClO溶液和0.1 mol·L-1CH3COONa溶液的pH |
比较HClO和CH3COOH的酸性强弱 |
| B |
向盛有1mL硝酸银溶液的试管中滴加NaCl溶液,至不再有沉淀生成,再向其中滴加Na2S溶液 |
说明一种沉淀能转化为另一种溶解度更小的沉淀 |
| C |
向NaAlO2溶液中滴加饱和NaHCO3溶液,有白色沉淀产生 |
验证两者都发生了水解反应,且相互促进 |
| D |
室温下,分别向2支试管中加入相同体积、相同浓度的Na2S2O3溶液,再分别加入相同体积不同浓度的稀硫酸 |
研究浓度对反应速率的影响 |
亮菌甲素为利胆解痉药适用于急性胆囊炎治疗等,其结构简式如图所示。下列有关叙述正确的是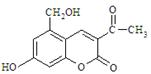
| A.亮菌甲素分子式为C12H11O5 |
| B.亮菌甲素能与三氯化铁溶液发生显色反应 |
| C.1mol亮菌甲素在一定条件下与NaOH溶液完全反应最多能消耗2mol NaOH |
| D.每个亮菌甲素分子在一定条件下与足量H2反应后的产物有3个手性碳原子 |