某温度时,Ag2SO4在水溶液中的沉淀溶解平衡曲线如图所示:下列有关Ag2SO4说法正确的是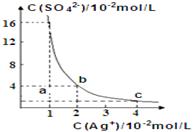
| A.含有大量SO42-的溶液中肯定不存在Ag+ |
| B.Ag2SO4的溶度积常数(Ksp)为8×10-4 |
| C.a点表示Ag2SO4的不饱和溶液,蒸发可以使溶液由a点变到b点 |
| D.0.02mol•L-1的AgNO3溶液与0.2mol•L-1的Na2SO4溶液等体积混合不会生成沉淀 |
全世界每年铜的产量为8×106t,工业上由辉铜矿(主要成分是Cu2S,其中铜元素为+1价)生产铜的主要反应为:Cu2S+O2 2Cu+SO2下列说法正确的是()
2Cu+SO2下列说法正确的是()
| A.该反应中Cu2S只是还原剂 |
| B.每生产1molCu需转移2mol电子 |
| C.该反应中Cu2S既是氧化剂又是还原剂 |
| D.若用该反应生产铜,全世界每年产生的SO2的体积 为1.4×106L |
有一种粉末它是由铁的氧化物中的一种或者两种组成,取3.04 g粉末加热,同时通入足量的CO使之完全反应,再用过量澄清石灰水把生成气体充分吸收,产生沉淀 5g。
则该粉末组成是()
| A.只有Fe2O3 | B.只有FeO |
| C.等物质的量的Fe2O3和Fe3O4 | D.等物质的量的FeO和Fe3O4 |
硝酸铜是制备Cu—Zn—Al系催化剂的重要原料。现有三种制取硝酸铜的实验方案可供选用
①铜与稀硝酸反应制取:3Cu+8HNO3(稀) 3Cu(NO3)2+2NO↑+4H2O
3Cu(NO3)2+2NO↑+4H2O
②铜与浓硝酸反应制取:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O
③首先将铜屑在空气中加热生成氧化铜,氧化铜与稀硝酸反应制取:
2Cu+O2 2CuO,CuO+2HNO3=Cu(NO3)2+H2O
2CuO,CuO+2HNO3=Cu(NO3)2+H2O
下列说法正确的是()
| A.制取等量的硝酸铜,需硝酸的量②最少 |
| B.制取等量的硝酸铜,②产生的有毒气体比①少 |
| C.三种方案中,硝酸的利用率为③>①>② |
| D.三种方案的反应都可以在铁质容器中进行 |
常温时,下列三个反应都能向右进行:
2W +X
+X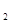
 2X
2X +W
+W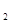
2Y +W
+W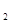
 2W
2W +Y
+Y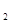
2X +Z
+Z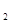
 2Z
2Z +X
+X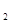
由此得出的正确结论是( )
A.X 、Y 、Y 、Z 、Z 、W 、W 中Z 中Z 的还原性最强 的还原性最强 |
B.X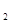 、Y 、Y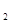 、Z 、Z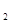 、W 、W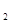 中Z 中Z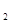 的氧化性最弱 的氧化性最弱 |
C.2Z +Y +Y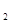  2Y 2Y +Z +Z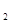 不能向右进行 不能向右进行 |
D.还原性X >Y >Y |
2L甲气体和1L乙气体恰好完全反应生成2L丙气体(所有气体的体积均在标准状况下测定)。若丙气体的化学式是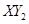 ,则甲、乙的化学式分别可能是()
,则甲、乙的化学式分别可能是()
A. 和 和 |
B.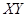 和 和 |
C. 和 和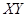 |
D.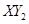 和 和 |