下列物质之间的转化都一步能实现的是
| A.Si→SiO2→H2SiO3→Na2SiO3 |
| B.Al→Al2O3→Al(OH)3→NaAlO2 |
| C.N2→NH3→NO→NO2→HNO3→NO2 |
| D.S→SO3→H2SO4→SO2→Na2SO3→Na2SO4 |
下列各组试剂(括号内的是滴加试剂)做溶液导电性实验的过程中,可以观察到灯泡由亮变暗直至熄灭,然后又逐渐变亮的是()
| A.NaOH溶液(稀硫酸) | B.氨水(醋酸溶液) |
| C.Ba(OH)2溶液(Ba(HCO3)2溶液) | D.醋酸溶液(醋酸钠溶液) |
下列曲线中,可以描述乙酸(甲,Ka=1.8×10-5)和一氯乙酸(乙,Ka=1.4×10-3)在水中的电离度与浓度关系的是()
将E和F加入密闭容器中,在一定条件下发生反应:E(g)+F(s) 2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示。
2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示。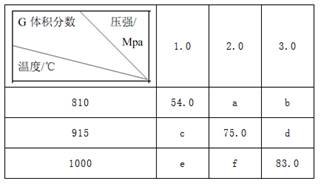
①b<f;②915℃、2.0MPa时E的转化率为60%;③该反应的ΔS>0;④K(1000℃)>K(810℃)
上述①~④中正确的有( )
| A.4个 | B.3个 | C.2个 | D.1个 |
温度为T时;向2.0 L恒容密闭容器中充入1.0 mol PCl5;反应PCl5(g)  PCl3(g)+Cl2(g)经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
PCl3(g)+Cl2(g)经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
| t/s |
0 |
50 |
150 |
250 |
350 |
| n(PCl3)/mol |
0 |
0.16 |
0. 19 |
0.20 |
0.20 |
下列说法正确的是()
A.反应在前50 s的平均速率v(PCl3)="0.0032" mol·L-1·s-1
B.保持其他条件不变;升高温度;平衡时c(PCl3)="0.11" mol·L-1;则反应的ΔH<0
C.相同温度下;起始时向容器中充入1.0 mol PCl5、0.20 mol PCl3和0.20 mol Cl2;反应达到平衡前v(正)>v(逆)
D.相同温度下;起始时向容器中充入2.0 mol PCl3和2.0 mol Cl2;达到平衡时;PCl3的转化率小于80%
一定条件下,通过下列反应可以制备特种陶瓷的原料MgO, MgSO3(s) + CO(g)  MgO(s) + CO2(g) +SO2(g) △H>0该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是()
MgO(s) + CO2(g) +SO2(g) △H>0该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是()
| 选项 |
x |
y |
| A |
温度 |
容器内混合气体的密度 |
| B |
CO的物质的量 |
CO2与CO的物质的量之比 |
| C |
SO2的浓度 |
平衡常数K |
| D |
MgSO4的质量(忽略体积) |
CO的转化率 |