某反应过程中的能量变化如图所示,则该反应的△H为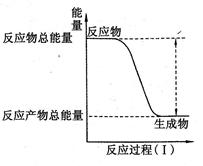
| A.△H>O | B.△H<O | C.△H="O" | D.无法判断 |
选考[选修3——物质结构与性质]
下列叙述正确的是
| A.SO32-中硫原子的杂化方式为sp3 |
| B.H2O分子中氧原子的杂化方式为sp2 |
| C.BF3分子呈三角锥体空间型 |
| D.C2H2分子中含有3个σ键和2个π键 |
选考[选修5——有机化学基础]
羟基扁桃酸是药物合成的重要中间体,它可由苯酚和乙醛酸在一定的条件下反应制得。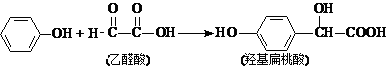
下列有关说法正确的是学
| A.该反应是取代反应 |
| B.苯酚和羟基扁桃酸遇上FeCl3溶液都会显色 |
| C.乙醛酸与H2加成的产物能在催化剂作用下形成高分子化合物 |
| D.1 mol羟基扁桃酸能与3 mol NaOH反应 |
某二次电池充、放电的化学方程式为:2K2S2+KI3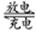 K2S4+3KI。与其它设备连接的电路如图示。当闭合开关K时,X附近溶液先变红。则下列说法正确的是
K2S4+3KI。与其它设备连接的电路如图示。当闭合开关K时,X附近溶液先变红。则下列说法正确的是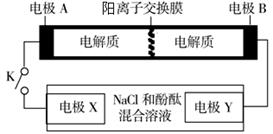
| A.K+从右到左通过离子交换膜 |
| B.A的电极反应式为:3I--2e-= I3- |
| C.当有0.1 mol K+通过离子交换膜,X电极上产生气体1.12 L(标准状况下) |
| D.电池充电时,B电极要与外电源的正极相连,电极上发生还原反应 |
硫酸亚锡(SnSO4)是一种重要的能溶于水的硫酸盐,广泛应用于镀锡工业。SnSO4的实验室制备设计路线如下: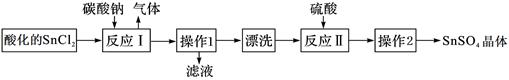
下列有关说法正确的是
| A.SnCl2酸化是为了防止溶解时发生水解 |
| B.反应I中发生的离子反应为:CO32-+2H+=CO2↑+ H2O |
| C.漂洗时,将固体置于烧杯中,加蒸馏水洗涤过滤2~3次 |
| D.操作1为过滤,操作2为结晶 |
用图中装置进行实验,实验一段时间后,现象与预测不一致的是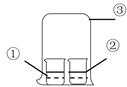
| ①中物质 |
②中物质 |
实验预测 |
|
| A |
浓氨水 |
酚酞试液 |
②中溶液变为红色 |
| B |
浓硝酸 |
淀粉KI溶液 |
②中溶液变为蓝色 |
| C |
浓盐酸 |
浓氨水 |
大烧杯中有白烟 |
| D |
饱和的亚硫酸溶液 |
稀溴水 |
②中无明显变化 |