常温下,0.1 mol·L-1CH3COONa溶液pH =a,则下列说法正确的是
| A.CH3COOH在常温下Ka数值约为l×101-2a |
| B.约有1.0×l0a-14 mol·L-1的水发生电离 |
| C.加热后溶液pH <a |
| D.加少量水后,溶液pH >a |
A、B为同主族的两元素,A在B的上一周期,若A的原子序数为n,则B的原子序数不可能为
A.n+8B.n+18C.n+32D.n+20
下列电子式书写正确的是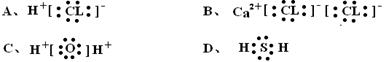
新制氯水与久置的氯水相比较,下列结论不正确的是
| A.颜色相同 | B.前者能使有色布条褪色 |
| C.都含有H+ | D.加AgNO3溶液都能生成白色沉淀 |
短周期金属元素甲~戊在元素周期表中的相对位置如下表所示,下面判断正确的是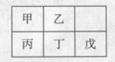
| A.原子半径:丙<丁<戊 | B.金属性:甲>丙 |
| C.氢氧化物碱性:丙>丁>戊 | D.最外层电子数:甲>乙 |
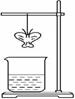
某同学用滤纸折成一个纸蝴蝶并喷洒一种溶液(保持湿润),挂在铁架台上。另取一只盛某种溶液的烧杯,放在纸蝴蝶的下方(如图)。过一会,发现纸蝴蝶变为蓝色。下表的组合中,能够实现上述变化的是
| A |
B |
C |
D |
|
| 纸蝴蝶上的喷洒液 |
酚酞 |
石蕊 |
石蕊 |
酚酞 |
| 小烧杯中的溶液 |
浓盐酸 |
NaOH溶液 |
浓氨水 |
浓硫酸 |
| A |
B |
C |
D |
|
| 纸蝴蝶上喷洒液 |
酚酞 |
石蕊 |
KI-淀粉溶液 |
品红 |
| 小烧杯中的溶液 |
浓氨水 |
浓盐酸 |
浓氯水 |
浓硫酸 |