下列离子方程式的书写及评价均合理的是
| 选项 |
离子方程式 |
评价 |
| A |
将2 mol Cl2通入到含1 mol FeI2的溶液中: 2Fe2++2I-+2Cl2===2Fe3++4Cl-+I2 |
正确; Cl2过量,Fe2+、I-均被氧化 |
| B |
用Cu电极电解NaCl溶液,阳极的电极反应式: 2Cl--2e-===Cl2↑ |
正确; Cl-优先于OH-放电 |
| C |
过量SO2通入到NaClO溶液中: SO2+H2O+ClO-===HClO+HSO3- |
正确; H2SO3的酸性强于HClO |
| D |
Mg(HCO3)2溶液与足量的NaOH溶液反应: Mg2++2HCO3-+4OH-="==" Mg(OH)2 ↓+ 2CO32-+2 H2O |
正确; Mg(OH)2比MgCO3更难溶 |
某溶液中,若忽略水的电离,只含有下表中所示的四种离子,试推测X离子及其个数b可能为
| 离子 |
Na+ |
Fe3+ |
Cl- |
X |
| 个数 |
3a |
2a |
a |
b |
A.NO3-、4 a B.SO42-、4 a C.OH-、8 a D.SO42-、8 a
分类方法在化学学科发展中起到了非常重要的作用。下列分类标准合理的是:①根据酸分子中含有的H原子个数将酸分为一元酸、二元酸等;②根据反应中是否有电子的转移将化学反应分为氧化还原反应和非氧化还原反应;③根据分散系是否具有丁达尔现象将分散系分为溶液、胶体和浊液;④根据水溶液能否导电可将物质分为电解质和非电解质
| A.①③ | B.①②④ | C.② | D.①②③④⑤ |
小美在奥运五连环中填入了5种物质,相连环物质间能发生反应,不相连环物质间不能发生反应。你认为“五连环”中物质间发生的反应,没有涉及的基本反应类型和属于氧化还原反应的个数有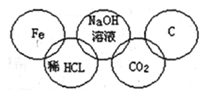
| A.复分解反应、1个 | B.分解反应、2个 |
| C.化合反应、3个 | D.置换反应、2个 |
在强酸性溶液中能大量共存的无色透明离子组是( )
A.K+、Na+、NO 、MnO 、MnO |
B.Mg2+、Na+、Cl-、SO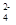 |
| C.K+、Na十、Br-、Cu2+ | D.Na十、Ba2+、OH-、SO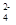 |
下列有关物质保存的说法正确的组合是()
①钠应该密封在煤油中保存;②过氧化钠可以露置在空气中保存;③氯水应该密封在无色试剂瓶中保存;④漂白粉不能露置在空气中保存。
| A.①③ | B.①②③④ | C.①③④ | D.①④ |