下列实验操作正确的是
| A.固体碘与NH4Cl的混合物可以用加热升华的方法分离 |
| B.过滤时,慢慢地将液体直接倒入过滤器中。 |
| C.可以用米汤检验含碘食盐中的碘元素 |
| D.水银洒落时,可在其表面覆盖一层硫粉进行处理。 |
下列关于离子的检验方法一定正确的是
| A.向某溶液中滴加BaCl2溶液,若有白色沉淀,则滴加足量稀HNO3,若有沉淀不溶解,则说明原溶液中一定含Ag+ |
| B.向某溶液中滴加浓NaOH溶液,产生的气体使湿润的红色石蕊试纸变蓝色,说明原溶液中含有NH4+ |
| C.向某溶液中滴加足量稀HCl,产生气体使澄清石灰水变浑浊,则说明原溶液中一定含CO32- |
| D.用铂丝蘸取某溶液在无色火焰上灼烧直接观察火焰颜色未见紫色,则说明原溶液中不含K+ |
某溶液中可能含有Na+、NH4+、Ba2+、SO42-、I-、S2-。分别取样:①用pH计测试,溶液显弱酸性;②加氯水和淀粉无明显现象.为确定该溶液的组成,还需检验的离子是
| A.SO42- | B.Na+ | C.Ba2+ | D.NH4+ |
下列实验现象预测正确的是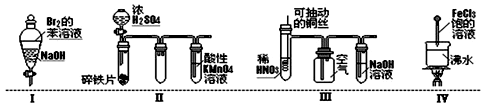
| A.实验Ⅰ:振荡后静置,溶液不再分层,且保持无色透明 |
| B.实验Ⅱ:铁片最终完全溶解,且高锰酸钾溶液变无色 |
| C.实验Ⅲ:微热稀HNO3片刻,溶液中有气泡产生,广口瓶内始终无明显变化 |
| D.实验Ⅳ:当溶液至红褐色,停止加热,让光束通过体系时可产生丁达尔现象 |
除去下列物质中所含的杂质,选用的试剂正确的是
| 选项 |
物质(杂质) |
试剂 |
| A |
食盐(细沙) |
NaOH溶液 |
| B |
CO(NH3) |
浓H2SO4 |
| C |
CO2(SO2) |
Na2CO3溶液 |
| D |
NaHCO3溶液(Na2CO3) |
Ca(OH)2溶液 |
NA代表阿伏加德罗常数的值。下列说法正确的是
| A.12g石墨和C60的混合固体中,含有NA个碳原子 |
| B.标准状况下,2.24L水中含有0.1NA个水分子 |
| C.7.8g过氧化钠含有的共用电子对数为0.2NA |
| D.5.6g铁在足量氯气中燃烧,电子转移数目为0.2NA |