某同学用以下装置制备并检验Cl2的性质。下列说法正确的是
| A.Ⅰ图:若浓盐酸过量,则理论上MnO2可全部消耗完 |
| B.Ⅱ图:证明新制氯水只具有酸性 |
| C.Ⅲ图:产生了棕黄色的雾 |
| D.Ⅳ图:湿润的有色布条褪色,说明氯气具有漂白性 |
某元素原子的质量数为A,它的阴离子Xn-核外有x个电子,w克这种元素的原子核内中子数为
A. |
B.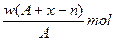 |
C. |
D. |
 和
和 在一定条件下充分反应后,得到的产物为
在一定条件下充分反应后,得到的产物为
A. 和 和 |
B. 和 和 |
C. 和 和 |
D. 和 和 |
下列反应属于取代反应的是
A. |
B. |
C.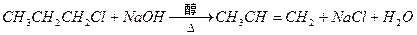 |
D. |
下列说法正确的是
| A.淀粉、纤维素、油脂、蛋白质都属于天然高分子形成的混合物 |
B.蔗糖溶液中加入新制 浊液煮沸会析出红色沉淀 浊液煮沸会析出红色沉淀 |
C.纤维素、淀粉都可用 表示,但它们并不为同分异构体 表示,但它们并不为同分异构体 |
| D.人体的各种组织的蛋白质不断分解,最终生成二氧化碳和水,排出体外 |
下列转化不属于煤或石油的综合利用的是
| A.将煤干馏制得煤焦油和焦炭 |
| B.在一定条件下将煤与氢气转化为液体燃料 |
| C.将煤变为煤饼作燃料 |
| D.将石油裂解制得乙烯等化工原料 |