2.0 mol PCl3和1.0 mol Cl2充入体积不变的密闭容器中,在一定条件下发生下述反应:PCl3(g)+Cl2(g) PCl5(g) 达平衡时PCl5为0.40 mol,如果此时再加入2.0 mol PCl3和1.0 mol Cl2,在相同温度下再达平衡时PCl5的物质的量是
PCl5(g) 达平衡时PCl5为0.40 mol,如果此时再加入2.0 mol PCl3和1.0 mol Cl2,在相同温度下再达平衡时PCl5的物质的量是
| A.小于0.40 mol | B.大于0.80 mol |
| C.等于0.80 mol | D.大于0.40 mol,小于0.80 mol |
固体氧化物燃料电池是由美国西屋(Westinghouse)公司研制开发的。它以固体氧化锆氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过。该电池的工作原理如下图所示,其中多孔电极a、b均不参与电极反应。下列判断正确的是()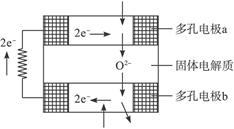
| A.有O2放电的a极为电池的负极 |
| B.有H2放电的b极为电池的正极 |
| C.a极对应的电极反应为O2+2H2O+4e-====4OH- |
D.该电池的总反应方程式为2H2+O2 2H2O 2H2O |
用惰性电极电解M(NO3)x的水溶液,当阴极上增重a g时,在阳极上同时产生b L O2(标准状况),从而可知M的相对原子质量为()
A. |
B. |
C.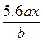 |
D. |
用石墨作电极电解100 mL H2SO4与CuSO4的混保液,通电一段时间后,两极均收集到2.24 L气体(标准状况),则原混合液中Cu2+的物质的量浓度为()
| A.1 mol·L-1 | B.2 mol·L-1 | C.3 mol·L-1 | D.4 mol·L-1 |
用石墨作电极电解1 L 1 mol·L-1 CuSO4溶液,当c(Cu2+)="0.5" mol·L-1时,停止电解,向剩余溶液中加入下列何种物质可使电解质溶液恢复至原来状况()
| A.CuSO4 | B.CuO | C.Cu(OH)2 | D.CuSO4·5H2O |
X、Y、Z、M代表四种金属元素。金属X和Z用导线连接放入稀硫酸中时,X溶解,Z极上有氢气放出;若电解Y2+和Z2+共存的溶液时,Y先析出;又知M2+的氧化性强于Y2+。则这四种金属的活动性由强到弱的顺序为()
| A.X>Z>Y>M | B.X>Y>Z>M | C.M>Z>X>Y | D.X>Z>M>Y |