常温下,取一定量的PbI2固体配成饱和溶液 ,T时刻改变某一条件,离子的浓度变化如图所示,(注:第一次平衡时c(I-)=2x10-3mol/L, c(Pb2+)=1x10-3mol/L)下列有关说法正确的是
| A.常温下,Ksp=2x10-6 |
| B.温度不变,向PbI2饱和溶液中加入少量硝酸铅浓溶液,PbI2的溶解度不变,c(Pb2+)不变 |
| C.T时刻改变的条件是升高温度,PbI2的,Ksp 增大 |
D.常温下Ksp[PbS]=8x10-28,向PbI2的悬浊液中加入Na2S溶液,PbI2(s)+S2-(aq) PbS(s)+2I-(aq)反应的化学平衡常数为5x1018 PbS(s)+2I-(aq)反应的化学平衡常数为5x1018 |
在稀氨水溶液中存在如下平衡体系:NH3·H2O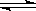 NH4++OH-,当增大溶液的pH时,c(NH4+)会()
NH4++OH-,当增大溶液的pH时,c(NH4+)会()
| A.可能增大也可能减小 | B.增大 |
| C.减小 | D.无变化 |
将下列四组溶液在烧杯中分别同时迅速混合,此时,硫代硫酸钠和盐酸缓慢地进行反应,则出现浑浊的先后顺序是()
① 20℃ 10mL 5.4mol/L的Na2S2O3溶液和20mL 1.5mol/L盐酸 ② 20℃ 10mL 4.0mol/L的Na2S2O3溶液和10mL 2.0mol/L盐酸③ 30℃ 15mL 3.5mol/L的Na2S2O3溶液和10mL 2.5mol/L盐酸 ④ 30℃ 20mL 3.0mol/L的Na2S2O3溶液和10mL 3.0mol/L盐酸
| A.③④②① | B.①②③④ | C.④③②① | D.④①③② |
若溶液中由水电离产生的c(OH-)=1×10-14 mol∙L-1,满足此条件的溶液中一定可以大量共存的离子组是
| A.Al3+、Na+、NO3-、Cl- | B.K+、Na+、Cl-、NO3- |
| C.K+、Na+、Cl-、AlO2- | D.K+、NH4+、SO42-、NO3- |
某温度下的定容密闭容器中,进行可逆反应:A(s)+2B(g) 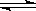 C(g)+D(g),当下列物理量不发生变化时: ①混合气体的密度 ②容器内气体的压强 ③混合气体的平均相对分子质量 ④B的物质的量浓度 则能表明该反应一定已达到平衡状态的是()
C(g)+D(g),当下列物理量不发生变化时: ①混合气体的密度 ②容器内气体的压强 ③混合气体的平均相对分子质量 ④B的物质的量浓度 则能表明该反应一定已达到平衡状态的是()
| A.只有④ | B.②③ | C.②③④ | D.①③④ |
已知反应:①101kPa时,C(s)+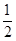 O2(g)═CO(g)△H1=-110.5kJ/mol
O2(g)═CO(g)△H1=-110.5kJ/mol
②稀溶液中,H+(aq)+OH-(aq)═H2O(l)△H2=-57.3kJ/mol,下列说中正确的是()
A.若碳的燃烧热用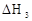 表示,则△H3<△H1 表示,则△H3<△H1 |
B.若碳的燃烧热用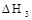 表示,则△H3>△H1 表示,则△H3>△H1 |
C.浓硫酸与稀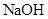 溶液反应的中和热值为57.3kJ·mol-1 溶液反应的中和热值为57.3kJ·mol-1 |
D.稀醋酸与稀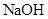 溶液反应生成1mol水,放出57.3kJ的热量 溶液反应生成1mol水,放出57.3kJ的热量 |