(14分)已知三氯化铁的熔点为306℃,沸点为315℃,易溶于水并且有强烈的吸水性,能吸收空气里的水分而潮解。某学习小组的同学对氯气与铁的反应及产物做了如下探究实验:
(1)装置的连接顺序为 。
(2)饱和食盐水的作用是 。
(3)反应一段时间后熄灭酒精灯,冷却后将硬质玻璃管及收集器中的物质一并快速转移至锥形瓶中,加入过量的稀盐酸和少许植物油(反应过程中不振荡),充分反应后,进行如下实验: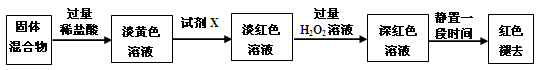
①淡黄色溶液中加入试剂X生成淡红色溶液的离子反应方程式为_______。
②淡红色溶液中加入过量H2O2后溶液红色加深的原因是 。
(4)已知红色褪去的同时有气体生成,经检验为O2。该小组同学对红色褪去的原因进行探究。
①取褪色后溶液三份,第一份滴加FeCl3溶液无明显变化;第二份滴加试剂X,溶液出现红色;第三份滴加稀HCl和BaCl2溶液,产生白色沉淀。
②另取同浓度的FeCl3溶液滴加2滴试剂X,溶液变红,再通入O2,无明显变化。
实验①说明 ;
实验②的目的是 ;
得出结论:溶液褪色的原因是 。
(14分)高锰酸钾俗称PP粉,为强氧化剂,遇到有机物就放出活性氧。这种氧有杀灭细菌的作用,且杀菌能力极强。某学生欲在实验室配制1 L 0.06 mol/L KMnO4稀溶液,用来清洗伤口。
(1)实验过程中需用托盘天平称取KMnO4晶体的质量为__________g。
(2)其操作步骤如下图所示,则右图所示操作应在下图中__________(填选项字母)之间。
A.②与③ B.①与② C.④与⑤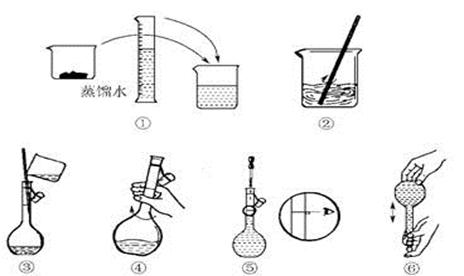
(3) 配制过程中需要用到的仪器有:托盘天平、药匙、烧杯、、、
(4)若该同学在配制溶液时,进行了如下操作,其中使所配溶液浓度偏低的操作
有_______________(填选项字母)。
A.称量KMnO4晶体时,指针偏向右边
B.将KMnO4晶体放在烧杯中溶解,冷却后,转移至含有少量蒸馏水的容量瓶中
C.定容时,仰视刻度线
D.振荡摇匀后,发现溶液液面低于刻度线,再滴加少量蒸馏水至刻度线处
盐酸、硝酸都是用途相当广泛的两种酸。
(1)瑞典科家舍勒在研究软锰矿(主要成份为MnO2)时,将浓盐酸与软锰矿混合加热,产生了一种有刺激性气味的有色气体。写出该反应的化学方程式,并标出电子转移方向和数目: 。
(2)某校合作学习探究小组学习科学家探究精神对氯气性质进行了探究,设计了以下一些实验。
| 实验内容 |
实验现象 |
|
| A |
收集一集气瓶气体,观察颜色,然后向瓶内倒入约占瓶容积1/5的蒸馏水,充分振荡。 |
蒸馏水呈浅黄绿色,瓶内气体仍呈黄绿色。 |
| B |
取出瓶内部分溶液,滴入紫色石蕊试液中直至过量。 |
紫色石蕊试液先变红色,后红色褪色。 |
| C |
取出瓶内剩下的部分溶液,滴入硝酸银溶液中。 |
产生大量白色沉淀 |
| D |
最后向瓶内倒入少量浓氢氧化钠溶液,振荡。 |
瓶内黄绿色气体立即消失。 |
①能说明氯气与水发生化学反应的实验是(填实验序号)
②写出实验D中所发生反应的离子方程式。
(3)该校另一合作学习探究小组用下列左图所示装置对铜与硝酸反应进行探究。
①甲同学观察到试管中的气体由无色变成了红棕色,由此认为试管里的硝酸是浓硝酸,你认为他的看法正确吗?。为什么?。
甲同学还能观察到的现象有。
②乙同学向反应完成后的溶液里滴加氢氧化钠溶液,产生的沉淀(m/g)和加入溶液的体积(V/mL)的关系如上右图所示。请写出O-A段反应的离子方程式 。
为研究某铁质材料与浓硫酸反应生成气体的成分,某学习小组进行了以下探究活动:
(1)称取铁钉5.6g放入20mL足量浓硫酸中,加热,理论上收集到气体SO2L(标况)。将所得气体全部通入足量溴水中,然后加入足量BaCl2溶液,经适当操作后得干燥固体23.3g。由此推知实际生成气体SO2的体积为L(标况)。
(2)分析上述实验中SO2体积的结果,有同学认为所得气体中除含有 SO2外,还可能含有H2和Q气体。为此设计了下
SO2外,还可能含有H2和Q气体。为此设计了下 列探究实验装置(图中夹持仪器省略)。
列探究实验装置(图中夹持仪器省略)。
①装置A中试剂的作用是
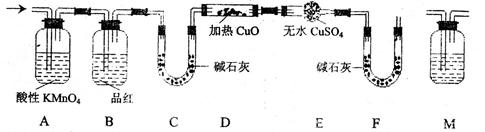
②认为气体中还含有的Q气体是
③为确认Q的存在,需在装置中添加M于,
a.A之前 b.AB之间 c.BC之间 d.CD之间
M中的试剂是
④如果气体中含有H2,预计实验现象应是
试回答下列问题:(1)下 列实验中所选用的仪器或操作以及结论不合理的是
列实验中所选用的仪器或操作以及结论不合理的是
A.用托盘天平称量11.7g氯化钠晶体
B.用碱式滴定管量取20.00mL Na2CO3溶液
C.加热NH4Cl晶体时,用湿润红色石蕊试纸靠近试管口,检验NH3的生成
D.测定溶液的pH时,用洁净、干燥的玻璃棒蘸取溶液,滴在用蒸馏水湿润过的pH试纸上与标准比色卡比较
E.仅用蒸馏水和pH试纸,就可以鉴别pH相等的H2SO4和CH3COOH溶液
(2)海洋植物海带中含有大量的碘 元素,碘元素以碘离子的形式存在。实验室里从海带中提取碘的流程如下图:
元素,碘元素以碘离子的形式存在。实验室里从海带中提取碘的流程如下图: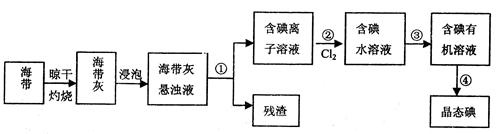
I.指出提取碘的过程中有关的实验操作名称:①,③
II.提取碘的过程中,可供选择的有机试剂是(填序号)
A.甲苯、酒精 B.四氯化碳、苯
C.汽油、乙酸 D.汽油、甘油
III.为使碘水溶液转化为碘的有机溶液,实验室有烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网以及必要的夹持仪器、物品,尚缺少的玻璃仪器有
氯气是一种重要的化工原料,自来水的消毒、农药的生产、药物的合成等都需要用到氯气。某化学兴趣小组欲采用图一装置制取氯气,并探究氯气的性质。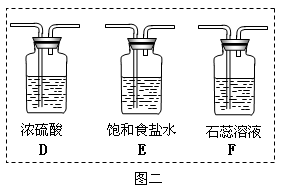
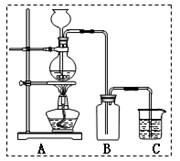
图一
(1)指出图一装置中的错误之处
(2)C装置中发生反应的离子方程式。
(3)为了制得干燥纯净的Cl2,请你结合图二将以上装置重新排序(可不选全):。
(4)如果实验室中MnO2用完了,则下列物质可能可以用来代替MnO2制Cl2的是。
| A.NaBiO3 | B.FeCl3 | C.PbO2 | D.Na2O2 |
已知氧化性强弱顺序为:NaBiO3>PbO2>MnO2>Na2O2>FeCl3
(5)为证明氯气的强氧化性,有同学将图一中的“B”换成“F”,你认为他这样做对吗?
。为什么?。