(12分)女贞四季常绿,枝叶茂密,树形整齐,是园林中常用的观赏树种。下图是根据女贞在不同温度条件下叶片净光合速率(用单位时间单位叶面积吸收的CO2量表示)的研究而绘制的坐标曲线。请据图回答下列问题:
(1)测定A点叶片净光合速率时,叶肉细胞释放的CO2来自_________,B点表示40℃条件下,叶肉细胞内的光合作用强度_________(填“>”、“=”或“<”)呼吸作用强度。
(2)与A点相比,B点叶肉细胞中特有的能量变化是_________,在此过程中,细胞吸收的CO2与五碳化合物结合形成的产物在酶、_________的参与下形成有机物。
(3)18℃条件下,在光照强度低于650umol/ 时,光合速率随____的增加而增大,此时光合速率主要受光合作用过程中____阶段的限制。
时,光合速率随____的增加而增大,此时光合速率主要受光合作用过程中____阶段的限制。
(4)40℃条件下,光照强度为650umol/ 时的光合速率为_________。由图可以看出,光照强度超过m点时,光合速率不再增加,影响这种变化的因素有________。
时的光合速率为_________。由图可以看出,光照强度超过m点时,光合速率不再增加,影响这种变化的因素有________。
某种植物是一濒危药用植物(二倍体)。请按要求回答问题:
(1)以该植物的茎尖和叶片为材料,通过组织培养获得了再生植株,解决了自然繁殖率低的问题。这表明植物细胞具有________。
(2) 在获取植物细胞的原生质体时,通常使用纤维素酶和果胶酶破除细胞壁,其原理是利用了酶的________性质。
(3)该植物自然结实率低,主要原因是花粉粒萌发后多数花粉管不能伸长。为探究生长素对植物花粉管伸长的影响,某生物兴趣小组进行了课外实验,得到下表结果:
| 生长素浓度(mg/L) |
0 |
1.0 |
2.0 |
3.0 |
4.0 |
5.0 |
6.0 |
7.0 |
| 花粉管平均长度(cm) |
0.5 |
3.5 |
5.5 |
6.4 |
5.2 |
3.1 |
0.4 |
0.2 |
请结合表中数据对实验结果进行简要分析:
①_____________________________________;
②_____________________________________;
③_____________________________________;
④_____________________________________。
根据上述分析,可以得出的结论是:_______________________。
根据所学知识回答:
(1)《长江日报》北京消息:我国首家“生命银行”——协和脐血干细胞自体储存库11日正式向市民开放,家长可把孩子出生时的脐血放在这里保存,当孩子日后万一患血液疾病或恶性肿瘤等症时,便可取出脐血为他移植治疗。从免疫学角度分析,脐血自身移植的优点有____________________。
(2)艾滋病没有有效的治疗药物。对艾滋病患者,药物只能改善和缓解症状,不可能治愈,对付艾滋病的办法只能是____。下列叙述中,哪些是正确的______(填序号)
① 遵守性道德,洁身自爱,正确使用安全套可以预防艾滋病;
② 坚决拒绝吸毒,尤其不共用注射器静脉吸毒可以预防艾滋病;
③ 共用牙刷、剃须(刮脸)刀不会传播艾滋病;
④ 同在一个教室上课,一起吃饭,一起玩耍会传播艾滋病;
⑤ 蚊子等昆虫叮咬不会传播艾滋病;
⑥ 可以随意泄露艾滋病患者和感染者的姓名、地址和个人隐私;
⑦ 不能以不正当理由拒绝为艾滋病患者和感染者提供服务,如购物、孩子上学、就医等。
(3)过敏反应是已免疫的机体在____接受相同物质的刺激时所发生的反应。在过敏原的刺激下,由____细胞产生的抗体吸附在皮肤、呼吸道或消化道黏膜以及血液中某些细胞的表面。预防过敏反应发生的主要措施是____________________。
根据所学知识填下表
| 比较项目 |
光合作用 |
有氧呼吸 |
化能合成作用 |
| 场所 |
(1) |
 (2) (2) |
|
| 物质变化 |
(3) |
(4) |
 |
| 能量转化 |
(5) |
 (6) (6) |
|
| 反应式 |
(7) |
(8) |
硝化细菌:(9) |
画概念图是将一组相关概念用线条和文字连接成图形,直观而形象的表示出这些概念之间的关系。请根据所学知识构建“特异性免疫”概念图(包括体液免疫和细胞免疫,概念之间的连接词)。
为研究高等动物的神经调节,科学家进行相关实验。请回答下列有关问题:
(1)在蛙的坐骨神经表面放置两个电极,连接到一个电表上(电表指针偏转方向代表电流方向)。静息时,电表没有测出电位差(如下图中①所示)。若在图①所示神经右侧的相应位置给予一适当的刺激,则电流表指针偏转的顺序依次为B→____。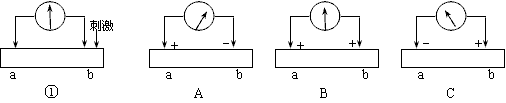
依据所观测到的电流表指针偏转情况,绘制出的电流变化情况曲线是下图中的__。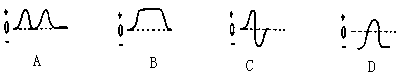
该实验表明:在一个神经元内,兴奋是以______的形式沿着神经纤维传导的。
(2)某反射弧结构完整,效应器为骨骼肌。科研人员用电极分别刺激传入神经和骨骼肌,同时用电流表分别记录传出神经的电流变化情况,则两次电流表的偏转情况依次为______、______。
(3)某研究人员通过实验分离获得两个蛙的心脏:第一个蛙心带有完整神经,第二个蛙心通过手术剔除全部神经。将两个蛙心都装上蛙心插管,并充以少量“任氏液”。持续刺激第一个蛙心脏的神经几分钟,发现心跳加速;随即将其中的任氏液吸出并转移到第二个未被刺激的蛙心脏内,发现后者的跳动也加速了。实验中的“任氏液”相当于蛙体内的____________(填成分名称),以维持蛙心正常的生理功能。根据该实验,可以做出的推断为____________________________________________________________。