能正确表示下列反应的离子方程式是
| A.Fe3O4与稀硝酸反应:Fe3O4+8H+=Fe2++2Fe3++4H2O |
| B.NaHSO4溶液与Ba(OH)2溶液反应至中性:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O |
| C.用CH3COOH溶解CaCO3:CaCO3+2H+=Ca2++H2O+CO2↑ |
| D.向FeCl2溶液中加入少量K3[Fe(CN)6]溶液:4Fe2++2[Fe(CN)6]4-=Fe4[Fe(CN)6]2↓ |
1.2g碳与适量水蒸气反应生成CO和H2,需吸收13.13KJ热量,此反应的热化学方程式为:
A.C + H2O ==CO + H2 ΔH== +131.3KJ·mol—1 +131.3KJ·mol—1 |
| B.C(s)+ H2O(g) ==CO(g) + H2(g) ΔH==+10.94KJ·mol—1 |
| C.C(s)+ H2O(l) ==CO(g) + H2(g) ΔH==+131.3KJ·mol—1 |
D.C(s)+ H2O(g) ==CO(g) + H2(g) ΔH==+131.3KJ·mol—1 ΔH==+131.3KJ·mol—1 |
在N2+3H2 2NH3的反应中,经过t秒钟后,H2的浓度增加了0.9mol/L,在此期间,正反应速率V(H2)=0.45mol/(L·S),则t值为:
2NH3的反应中,经过t秒钟后,H2的浓度增加了0.9mol/L,在此期间,正反应速率V(H2)=0.45mol/(L·S),则t值为:
| A. 1秒 | B. 1.5秒 | C. 2秒 . | D. 2.5秒 |
下列关于反应热的说法正确的是
| A.当∆H为负数时,表示该反应为吸热反应 |
B.已知C(s)+ O2(g)=CO(g) △H =-110.5kJ/mol,说明碳的燃烧热为110.5kJ O2(g)=CO(g) △H =-110.5kJ/mol,说明碳的燃烧热为110.5kJ |
| C.反应热的大小与反应物所具有的能量和生成物所具有的能量无关 |
| D.化学反应的反应热只与反应体系的始态和终点状态有关,而与反应的途径无关 |
下列变化属于吸热的化学反应是
①液态水汽化②将胆矾加热变为白色粉末③浓硫酸稀释④氯酸钾分解制氧气⑤生石灰跟水反应生成熟石灰
| A.①④⑤ | B.①②④ | C.②③ | D.②④ |
已知H2(g)+Cl2( g)="2HCl(g)" △H=―184.6kJ·mol-1,则反应HCl(g)=
g)="2HCl(g)" △H=―184.6kJ·mol-1,则反应HCl(g)=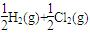 的△H为:
的△H为:
| A.+184.6kJ·mol-1 | B.―92.3kJ·mol-1 | C.―369.2kJ·mol-1 | D.+92.3kJ·mol-1 |