已知常温下CH3COOH的电离平衡常数为Ka ,常温下,向20mL 0.1 mol·L-1CH3COOH溶液中逐滴加入0.1 mol·L-1NaOH溶液,其pH变化曲线如图所示(忽略温度变化)。下列说法中正确的是
| A.a点表示的溶液中由水电离出的H+浓度为1.0×10-3mol·L-1 |
| B.b点表示的溶液c(CH3COO-)< c(Na+) |
C.b、d点表示的溶液中 相等 相等 |
| D.c点表示CH3COOH和NaOH恰好反应完全 |
用下图表示的一些物质或概念之间的从属或包含关系中,错误的是()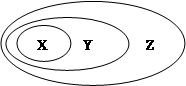
| X |
Y |
Z |
|
| 例 |
氧化物 |
化合物 |
纯净物 |
| A |
溶液 |
分散系 |
混合物 |
| B |
铜 |
金属元素 |
元素 |
| C |
强电解质 |
电解质 |
化合物 |
| D |
置换反应 |
氧化还原反应 |
离子反应 |
下列说法中,正确的是()
| A.化学科学与其他科学分支的联系不密切 |
| B.化学研究的主要目的就是认识分子 |
| C.化学家可以在微观层面上操纵分子和原子,组装分子材料、分子器件和分子机器 |
| D.化学研究会造成严重的环境污染。 |
在常温下,纯水中存在电离平衡H2O H++OH-,若要使水的电离平衡向电离方向移动,并使c(H+)增大,可加入的适当物质是()
H++OH-,若要使水的电离平衡向电离方向移动,并使c(H+)增大,可加入的适当物质是()
| A.硫酸氢钠 | B.明矾 | C.碳酸氢钠 | D.醋酸氢钠 |
NH4Cl溶于重水后,产生的一水合氨和水合氢离子均正确的是()
| A.NH2D·H2O、D3O+ | B.NH3·D2O、HD2O+ |
| C.NH3·HDO、D3O+ | D.NH2D·HDO、H2DO+ |
若pH=3的酸溶液和pH=11的碱溶液等体积混合后溶液呈酸性,其原因可能是()
| A.生成了一种强酸弱碱盐 | B.弱酸溶液和强碱溶液反应 |
| C.强酸溶液和弱碱溶液反应 | D.一元强酸溶液和一元强碱溶液反应 |