在密闭容器里,A与B反应生成C,其反应速率分别用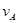 、
、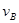 、
、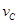 表示,已知2
表示,已知2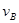 =3
=3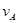 、3
、3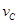 =2
=2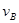 ,则此反应可表示为
,则此反应可表示为
| A.2A+3B=2C | B.A+3B=2C | C.3A+B=2C | D.A+B=C |
在体积可变的密闭容器中,反应mA(g)+nB(s) pC(g)达到平衡后,压缩容器的体积,发现A的转化率随之降低。下列说法中,正确的是( )。
pC(g)达到平衡后,压缩容器的体积,发现A的转化率随之降低。下列说法中,正确的是( )。
| A.(m+n)必定小于p | B.(m+n)必定大于p |
| C.m必定小于p | D.n必定大于p |
一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生NO2(g)+SO2(g) SO3(g)+NO(g)的可逆反应,下列能说明反应达到平衡状态的是()
SO3(g)+NO(g)的可逆反应,下列能说明反应达到平衡状态的是()
| A.体系压强保持不变 | B.混合气体颜色保持不变 |
| C.SO3和NO的体积比保持不变 | D.每消耗1 mol SO3的同时生成1 mol NO2 |
目前人类已发现的非金属元素除稀有气体外,共有16种。下列对这16种非金属元素的相关判断:①都是主族元素,最外层电子数都大于4;②单质在反应中都只能作氧化剂;③氢化物常温下都是气态,所以又都叫气态氢化物;④氧化物常温下都可以与水反应生成酸:
| A.只有②③正确 |
| B.只有①③正确 |
| C.只有④正确 |
| D.①②③④均不正确 |
下列关于Cl、N、S等非金属元素化合物的说法正确的是:
| A.漂白粉的成分是次氯酸钙 |
| B.实验室可用浓硫酸干燥氨气 |
| C.实验室可用NaOH 处理Cl2和HCl 废气 |
| D.Al2(SO4)3可除去碱性废水及酸性废水中的悬浮颗粒 |
下列除去杂质的实验方法正确的是:
| A.除去CO中少量O2:通过灼热的Cu网后收集气体 |
| B.除去K2CO3固体中少量NaHCO3:置于坩埚中加热 |
| C.用过量氨水除去Al3+溶液中的少量Fe3+ |
| D.除去FeCl3酸性溶液中少量的FeCl2:加入稍过量双氧水后放置 |