下列说法正确的是
| A.有气体参加的化学反应,若增大压强,可增加活化分子的百分数,从而使反应速率增大 |
| B.催化剂不参与反应,但能降低活化能增大活化分子的百分数,从而增大反应速率 |
| C.增大反应物浓度,可增大活化分子的百分数,从而使单位时间有效碰撞次数增多 |
| D.升高温度能使化学反应速率增大,主要原因是增大了反应物分子中活化分子的百分数 |
下列说法正确的是()
| A.增大压强,化学反应速率一定增大 |
| B.化学反应速率为反应时间内反应物浓度的增加或者生成物浓度的减少 |
| C.升高温度,化学反应速率一定增大 |
| D.加入反应物,化学反应速率增大 |
元素在周期表中的位置,反映了元素的原子结构和元素的性质,下列说法正确的是()
| A.同一元素不可能既表现金属性,又表现非金属性 |
| B.第三周期主族元素的最高正化合价等于它所处的主族序数 |
| C.短周期元素形成离子后,最外层都达到8电子稳定结构 |
| D.同一主族的元素的原子,最外层电子数相同,化学性质完全相同 |
下列有关化学用语的表示方法中正确的是()
A.氯元素的原子结构示意图: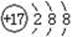 |
B.N2的结构式:N≡N |
C.原子核内有8个中子的氧原子: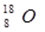 |
D.二氧化碳的电子式: |
下列反应属于吸热反应的是( )
| A.碳与水蒸气制水煤气的反应 |
| B.生石灰和水的反应 |
| C.盐酸与氢氧化钠溶液的反应 |
| D.木炭在氧气中燃烧 |
美国科学家将两种元素铅和氪的原子核对撞,获得了一种质子数118,中子数为175的超重
元素,该元素原子核内中子数与核外电子数之差是()
| A.57 | B.47 | C.61 | D.293 |