从薄荷油中得到一种烃A(C10H16),叫ɑ—非兰烃,与A相关反应如下:

(1)H的分子式为 。
(2)B所含官能团的名称为 。
(3)含两个—COOCH3基团的C的同分异构体共有 种(不考虑手性异构),其中核磁共振氢谱呈现2个吸收峰的异构体结构简式为 。
(4)B→D,D→E的反应类型分别为 、 。
(5)G为含六元环的化合物,写出其结构简式: 。
(6)F在一定条件下发生聚合反应可得到一种高级吸水性树脂,该树脂名称为 。
(7)写出E→F的化学方程式: 。
(8)A的结构简式为 ,A与等物质的量的Br2进行加成反应的产物共有 种(不考虑立体异构)。
有下列各组物质:
| A.O2和O3; | B.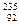 U和 U和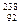 U; U; |
C.CH3CH2CH2CH3和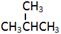 ; ; |
D.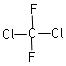 和 和 ; (E)甲烷和新戊烷 ; (E)甲烷和新戊烷 |
(1)___组两物质互为同位素;(2)___组两物质互为同素异形体;
(3)___组两物质互为同系物;(4)___组两物质互为同分异构体;
(5)___组两物质互为同一物质。
(11分)已知Ca(OH)2的溶解度随温度升高而降低。如下图所示,在试管中放入少许镁条,将试管浸入盛饱和石灰水的烧杯中,再向试管中滴入5mL 5mol · L-1盐酸。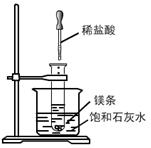
(1)实验中可观察到的现象有:
①_____________________ _ ______;
②__________________________________。
(2)试管中发生反应的离子方程式为______________________________。
(3)由实验推知,镁条和盐酸的总能量_________(填“大于”、“小于”或“等于”)MgCl2溶液和H2的总能量。判断的根据是_____________________。
某温度下,在2L容器中3种物质间进行反应, X、Y、Z的物质的量随时间的变化曲线如图。反应在t1min时到达平衡,依图所示: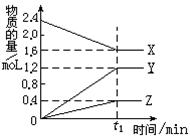
⑴①该反应的化学方程式是_____________________。
②在t1min时,该反应达到了__________状态,下列可作
为判断反应已达到该状态的是__________(填序号)。
| A.X、Y、Z的反应速率相等 | B.X、Y的物质的量浓度不再改变 |
| C.生成3molY的同时生成1molZ | D.生成1molZ的同时生成2molX |
⑵①若上述反应中X、Y、Z分别为NH3、H2、N2,且已知1mol氨气分解成氮气和氢气要吸收46kJ的热量,则由H2、N2合成NH3反应的热化学反应方程式为:
______________。
②甲、乙两位同学讨论放热反应和吸热反应:甲说加热后才能发生的化学反应是吸热反应;乙说反应中要持续加热才能进行的反应是吸热反应。你认为他们说法正确的是_____同学。
在一定条件下,向体积为2 L的容器中加入2 molO2和3 molSO2进行可逆反应:2SO2(g)+ O2(g) 2SO3(g),2 min后测得O2的物质的量为1.6 mol,则:
2SO3(g),2 min后测得O2的物质的量为1.6 mol,则:
(1)2 min内,SO2的物质的量减少了,SO3的物质的量增加了;
(2)若用O2的浓度变化来表示该反应的反应速率,则v(O2)=;
(3)若用SO3的浓度变化来表示该反应的反应速率,则v(SO3)=。
已知氢化钠(NaH)属于离子化合物,NaH跟水反应可以放出氢气。则
(1)NaH与水反应的化学方程式为,氧化剂为________,氧化产物为________,生成1mol H2转移电子mol;
(2)NaH中的两种离子,离子半径小的是_____ (填离子符号);
(3)如何通过实验证明NaH属于离子化合物?___________________________ 。