某兴趣小组设计如下微型实验装置。实验时,现断开K2,闭合K1,两极均有气泡产生;一段时间后,断开K1,闭合K2,发现电流表指针偏转,下列有关描述正确的是
A.断开K2,闭合K1时,总反应的离子方程式为:2H++2Cl— Cl2↑+H2↑ Cl2↑+H2↑ |
| B.断开K2,闭合K1时,石墨电极附近溶液变红 |
| C.断开K1,闭合K2时,铜电极上的电极反应为:Cl2+2e—=2Cl— |
| D.断开K1,闭合K2时,石墨电极作正极 |
在容积不变的密闭容器中有反应:X(g) + Y(g) 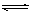 z(g),若Z(g)的物质的量浓度c(Z)与温度T的关系如图所示(曲线上的任意一点都表示平衡状态)。则下列说法不正确的是
z(g),若Z(g)的物质的量浓度c(Z)与温度T的关系如图所示(曲线上的任意一点都表示平衡状态)。则下列说法不正确的是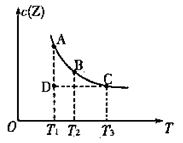
| A.A点与B点相比,B点的c (X)大 |
| B.A点与C点的化学反应速率:前者<后者 |
| C.在反应进行到D点时,V正〉V逆 |
| D.该反应的正反应是吸热反应 |
在铁制品上镀上一定厚度的铜,以下电镀方案中正确的是
| A.铜作阳极,铁制品作阴极,溶液中含Fe2+ |
| B.铜作阴极,铁制品作阳极,溶液中含Cu2+ |
| C.铜作阴极,铁制品作阳极,溶液中含Fe3+ |
| D.铜作阳极,铁制品作阴极,溶液中含Cu2+ |
在0.1mol·L-1 CH3COOH溶液中存在如下电离平衡:CH3COOH CH3COO-+H+,对于该平衡,下列叙述中,正确的是
CH3COO-+H+,对于该平衡,下列叙述中,正确的是
| A.加入水时,平衡向逆反应方向移动 |
| B.加入少量NaOH固体,平衡向正反应方向移动 |
| C.加入少量0.1 mol·L-1 HCl溶液,溶液中[ H+] 减小 |
| D.加入少量CH3COONa固体,平衡向正反应方向移动 |
下列电离方程式的书写中,正确的是
A.NaHS 溶于水::NaHS ==Na+ + HS- HS-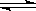 H+ + S2- H+ + S2- |
B.(NH4)2SO4溶于水: (NH4)2SO4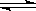 2NH4+ + SO42- 2NH4+ + SO42- |
| C.磷酸溶于水中::H3PO4 ="=" 3H+ + PO43- |
| D.Al(OH)3的电离::Al(OH)3 = Al3+ + 3OH- |
在一定温度下反应2NO2(g ) N2O4 ( g ) 已达到平衡,缩小此密闭容器的容积,则混合气体颜色的变化是
N2O4 ( g ) 已达到平衡,缩小此密闭容器的容积,则混合气体颜色的变化是
| A.变深 | B.变浅 | C.先变深再稍变浅 | D.先变浅再稍变深 |