将CO2慢慢通入一定体积的NaOH溶液中,溶液的pH随CO2体积(标准状况下)的变化曲线如图所示,则下列说法中正确的是
| A.NaOH溶液的物质的量浓度为0.1 mol/L,体积为1 L。 |
| B.M、N点离子浓度的都是c(HCO3-)>c(CO32-)。 |
| C.V=3.36 L时,溶液中的离子浓度关系是c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)。 |
| D.曲线上任意点都符合:c(Na+)+c(H+)=c(CO32-)+c(HCO3-)+c(OH-)。 |
下列有机物命名正确的是( )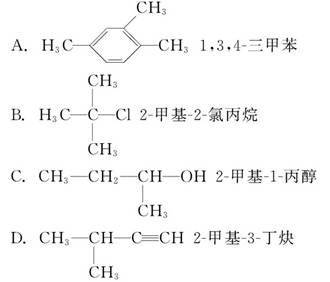
鲨鱼是世界上唯一不患癌症的动物,科学研究表明,鲨鱼体内含有一种角鲨烯,具有抗癌性。已知角鲨烯分子中含有30个碳原子及6个C=C且不含环状结构,则其分子式为()
| A.C30H60 | B.C30H56 | C.C30H52 | D.C30H50 |
某炔烃氢化后得到的饱和烃是: ,该烃可能的结构有( )
,该烃可能的结构有( )
| A.1种 | B.2种 | C.3种 | D.4种 |
下列说法中错误的是( )
①化学性质相似的有机物是同系物
②分子组成相差一个或几个CH2原子团的有机物是同系物
③若烃中碳、氢元素的质量分数相同,它们必定是同系物
④互为同分异构体的两种有机物的物理性质有差别,但化学性质必定相似
| A.①②③④ | B.只有②③ | C.只有③④ | D.只有①②③ |
有一类最简单的有机硅化合物叫硅烷,它的分子组成与烷烃相似。下列说法中错误的是( )
| A.硅烷的分子通式为SinH2n+2 | B.甲硅烷燃烧生成二氧化硅和水 |
| C.甲硅烷的密度大于甲烷 | D.甲硅烷的热稳定性强于甲烷 |