[化学——选修3:物质结构与性质](15分)A、B、C、D、E代表五种常见元素,它们的核电荷数依次增大。其中元素E的基态3d轨道上有2个电子,A的基态原子中有2个未成对电子,B是地壳中含量最多的元素,C是短周期中最活泼的金属元素, D与C可形成CD型离子化合物。请回答下列问题:
(1)E的基态原子价层电子排布式为 。
(2)AB2分子中,A的杂化类型为 ;在元素周期表中A、B及与两者紧邻的元素的第一电离能由大到小的顺序为(用元素符号表示) ;1个AB2分子中,含有 个∏键和 个δ键。
(3)AB2形成的晶体的熔点 (填“高于”“低于”或“无法判断”)CD形成的晶体的熔点,原因是 .
(4)E与B形成的一种橙红色晶体晶胞结构如图所示,其化学式为 (用元素符号表示)。 ED4是制取航天航空工业材料的重要原料。取上述橙红色晶体,放在电炉中,通入D2和A的单质后高温加热,可制得ED4,同时产生一种造成温室效应的气体,写出反应的化学方程式: .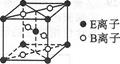
(5)由C、D两元素形成的化合物组成的晶体中,阴、阳离子都具有或近似具有球型对称结构,它们都可以看作刚性圆球,并彼此“相切”。如下图所示为C、D形成化合物的晶胞结构图以及晶胞的剖面图:若a=5.6×10-8cm,则该晶体的密度为 g·cm-3。(精确到小数点后1位)。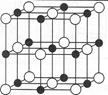
【化学——物质结构与性质】13分)
氮元素可以形成多种化合物。回答以下问题:
(1)基态氮原子的价电子排布式是_________________。
(2)C、N、O三种元素第一电离能从大到小的顺序是____________。
(3)肼(N2H4)分子可视为NH3分子中的一个氢原子被-NH2(氨基)取代形成的另一种氮的氢化物。
①NH3分子的空间构型是_______________;N2H4分子中氮原子轨道的杂化类型是___________。
②肼可用作火箭燃料,燃烧时发生的反应是:
N2O4(l)+2N2H4(l)===3N2(g)+4H2O(g) △H=-1038.7kJ·mol-1
若该反应中有4mol N-H键断裂,则形成的π键有________mol。
③肼能与硫酸反应生成N2H6SO4。N2H6SO4晶体类型与硫酸铵相同,则N2H6SO4的晶体内不存在__________(填标号)
a. 离子键 b. 共价键 c. 配位键 d. 范德华力
(4)图1表示某种含氮有机化合物的结构,其分子内4个氮原子分别位于正四面体的4个顶点(见图2),分子内存在空腔,能嵌入某离子或分子并形成4个氢键予以识别。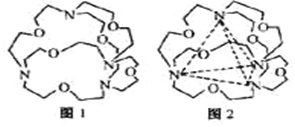
下列分子或离子中,能被该有机化合物识别的是_________(填标号)。
a. CF4 b. CH4 c. NH4+ d. H2O
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产.生活中有着重要作用。请回答下列问题:
(1)用CH4 催化还原NOx 可以消除氮氧化物的污染。例如:
CH4(g) + 4NO2(g) = 4NO(g)+CO2(g) + 2H2O(g)ΔH1=-574 kJ·mol-1
CH4(g) + 4NO(g) =" 2" N2(g)+CO2(g) + 2H2O(g)ΔH2、
若1 mol CH4 还原NO2 至N2,整个过程中放出的热量为867 kJ,则ΔH2=;
(2)工业合成氨气需要的反应条件非常高且产量低,而一些科学家采用高质子导电性的SCY陶瓷(能传递H+)实现氨的电化学合成,从而大大提高了氮气和氢气的转化率。电化学合成氨过程的总反应式为:N2+3H2 2NH3,则在电化学合成氨的过程中,阴极反应式为;
2NH3,则在电化学合成氨的过程中,阴极反应式为;
(3)在一定条件下,将l mol N2 与3 mol H2 混合于一个10 L密闭容器中,反应达到平衡时,A点混合气体中氨占25%,试回答:
①A点时N2的浓度为mol/L;
②右图中在状态A时,平衡常数 KA =(填写代入数值的表达式,不要求化简);当温度由T1变化到T2时,KA KB(填“>”、“<”或“=”)。
③在容积固定的密闭容器中发生上述反应,各物质的浓度如下表:
| 时间/min 浓度/mol•L—1 |
c (N2) |
c (H2) |
c (NH3) |
| 0 |
0.6 |
1.8 |
0 |
| 3 |
0.52 |
x |
0.16 |
| 6 |
0.36 |
1.08 |
0.48 |
| 9 |
0.36 |
1.08 |
0.48 |
反应从0 min到3 min之间,H2的反应速率为;反应在3 min时,条件发生了改变,改变的条件可能是(填序号)。
a.使用催化剂 b.降低温度 c.增加H2的浓度 d.充入Ne增大压强
A、B、C、D、E 五种短周期主族元素分占三个周期,A、B、C为同一周期依次相邻的3种元素,A和C的原子序数之比为3∶4,E原子的电子层数等于最外层电子数,D的原子序数小于E。请用化学用语回答相关问题:
(1)A元素在周期表中的位置。
(2)比较C和E简单离子半径大小:。
(3)元素E的一种常见的可溶性盐溶液呈碱性,其原因是(用离子方程式表示):;
(4)X、Y、Z、甲、乙、丙是由A、B、C分别与D形成的化合物,六种化合物可以排成下表,其中同一横行的分子中电子数相同,同一纵行的物质所含元素种类相同,其中X、Y、甲常温常压下为气体,Z、乙、丙常温常压下为液体。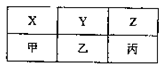
①甲的分子式为;丙的电子式为。
②乙的分子式为B2D4,乙和丙常作火箭推进器的燃料,反应后的产物无污染。已知8g液态乙与足量液态丙完全反应,产物均为气体时,放出热量为160.35kJ,试写出该反应的热化学方程式:。
【化学——选修5:有机化学基础】
甜樱桃中含有一种羟基酸(用A表示),A的碳链结构无支链,分子式为C4H6O5,1.34 g A与足量的NaHCO3溶液反应,生成标准状况下的气体0.448 L。A在一定条件下可发生如下转化:
其中,E的化学式为C4H6O6。已知: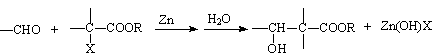
(X代表卤原子,R代表烃基),A的合成方法如下:
①F+BrCH2-COOCH2CH3 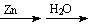 G+Zn(OH)Br
G+Zn(OH)Br
②G+2H2O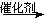 A +2M (其中,F、G、M分别代表一种有机物)
A +2M (其中,F、G、M分别代表一种有机物)
请回答下列问题:
(1)E的结构简式为___________,E的核磁共振氢谱中会出现组峰,一分子E最多能与几分子乙醇发生分子间脱水。
(2)从A到D所发生的化学反应的类型依次是。
(3)F的分子式是___________。写出满足下列条件的F的同分异构体的结构简式:①能与NaHCO3反应,且常温下能使溴水褪色;②不能发生银镜反应;③1摩该同分异构体与足量钠反应,标况下可得到22.4L氢气(注:羟基不能直接与双键相连)。。
(4)写出G与水反应生成A和M的化学方程式 。
【化学——选修3:物质结构与性质】
已知X、Y和Z三种元素的原子序数之和等于48。X的一种1∶2型氢化物分子中既有σ键又有π键,所有原子共平面。Z是金属元素,Z的单质和化合物有广泛的用途。已知Z的核电荷数小于28,且次外层有2个未成对电子。工业上利用ZO2和碳酸钡在熔融状态下制取化合物M(M可看做一种含氧酸盐)。经X射线分析,M晶体的最小重复单元为正方体(如上图),顶点位置为Z4+所占,体心位置为Ba2+所占,所有棱心位置为O2–所占。
(1)Y2+的结构示意图________________;Z的价层电子排布式为____________。
(2)X在该氢化物中以_____________方式杂化;X和Y形成的化合物YX2的电子式为_____________________。
(3)①制备M的化学反应方程式是______________________________________;
②在M晶体中,若将Z4+置于立方体的体心,Ba2+置于立方体的顶点,则O2–处于立方体的_______________;
③已知O2–半径为1.4×10–10 m,Z4+的半径为6.15×10–11m,阿佛加德罗常数为NA,则M的密度为_______________g·cm–3。(不必化简)