下列金属冶炼的反应原理,错误的是
A.2NaCl(熔融) 2Na+Cl2↑ 2Na+Cl2↑ |
B.MgO+H2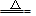 Mg+H2O Mg+H2O |
C.Fe3O4+4CO  3Fe+4CO2 3Fe+4CO2 |
D.2HgO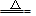 2Hg + O2↑ 2Hg + O2↑ |
有一化学平衡:mA(g)+nB(g) pC(g)+qD(g)(如右图)表示的是转化率与压强、温度的关系。分析图中曲线可以得出的结论是
pC(g)+qD(g)(如右图)表示的是转化率与压强、温度的关系。分析图中曲线可以得出的结论是
| A.正反应吸热:m+n>p+q |
| B.正反应吸热:m+n<p+q |
| C.正反应放热:m+n>p+q |
| D.正反应放热:m+n<p+q |
下列化合物属于弱电解质的是
| A.HClO4 | B.Ba(OH)2 | C.CO2 | D.HF |
已知反应X+Y= M+N为放热反应,对该反应的下列说法中正确的
| A.X的能量一定高于M |
| B.Y的能量一定高于N |
| C.X和Y的总能量一定高于M和N的总能量 |
| D.因该反应为放热反应,故不必加热就可发生 |
对已达化学平衡的下列反应 2X(g)+Y(g) 2Z(g)减小压强时,对反应产生的影响是
2Z(g)减小压强时,对反应产生的影响是
| A.逆反应速率增大,正反应速率减小,平衡向逆反应方向移动 |
| B.逆反应速率减小,正反应速率增大,平衡向正反应方向移动 |
| C.正、逆反应速率都减小,平衡向逆反应方向移动 |
| D.正、逆反应速率都增大,平衡向正反应方向移动 |
已知下列热化学方程式:
Zn(s)+1/2O2(g)===ZnO(s)ΔH1=-351.1 kJ/mol
Hg(l)+1/2O2(g)===HgO(s)ΔH2=-90.7 kJ/mol
由此可知Zn(s)+HgO(s)===ZnO(s)+Hg(l)ΔH3,其中ΔH3是
| A.-441.8 kJ/mol | B.-254.6 kJ/mol |
| C.-438.9 kJ/mol | D.-260.4 kJ/mol |