三草酸合铁酸钾晶体易溶于水,难溶于乙醇,可用作某些化学反应的催化剂,化学式为K3[Fe(C2O4)3]·3H2O。实验室以铁屑为原料制备三草酸合铁酸钾晶体相关反应过程如图所示:
请回答下列问题:
(1)制备过程中加入H2O2目的是______________,得到K3[Fe(C2O4)3]溶液后,需要加入乙醇,其目的是_________________。
(2)晶体中所含的结晶水可通过重量分析法测定,主要步骤有:①称量,②置于烘箱中脱结晶水,③冷却,④称量,⑤重复脱水、冷却、称量至恒重,⑥计算。步骤⑤的目的是___________________。
(3) 可被高锰酸钾溶液氧化放出CO2,测定产物中K3[Fe(C2O4)3]·3H2O含量时,可用酸性高锰酸钾标准溶液进行滴定。
可被高锰酸钾溶液氧化放出CO2,测定产物中K3[Fe(C2O4)3]·3H2O含量时,可用酸性高锰酸钾标准溶液进行滴定。
①写出滴定过程中发生反应的离子方程式_____________;
②取10.0g产物配成100mL溶液,从中取出20mL于锥形瓶中,用0.1mol·L-1的酸性高锰酸钾溶液进行滴定,达到滴定终点时消耗酸性高锰酸钾溶液24mL。则产物中K3[Fe(C2O4)3]·3H2O的质量分数为_________。(K3[Fe(C2O4)3]·3H2O相对分子质量为491)
Ⅰ.实验室制备硝基苯主要步骤如下:①配制一定比例的浓硫酸与浓硝酸的混合酸,加入反应器中。②向室温下的混合酸中逐滴加入一定量的苯,充分振荡,混合均匀。③在50℃至60℃下发生反应,直至反应结束。④除去混合酸后,粗产品依次用蒸馏水和5%NaOH溶液洗涤。⑤将用无水CaCl2干燥后的粗硝基苯进行蒸馏,得到纯硝基苯。
填写以下空白:
(1)配制一定比例浓硫酸和浓硝酸混合酸时,操作注意事项:___________________;
(2)操作③中,为了使反应在50℃至60℃下进行,常用的方法是:________________;
(3)步骤④中,分离粗硝基苯应使用的仪器是:________________________;
(4)步骤④中粗产品用5%NaOH溶液洗涤的目的是:___________________;
Ⅱ.某化学活动小组设计以下装置进行不同的实验。其中a为用于鼓入空气的气囊,b为螺旋状铜丝,c中盛有冰水。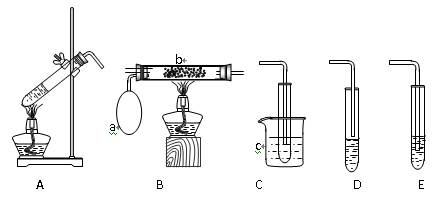
(1)若用A装置做乙醇与乙酸的酯化反应实验,则还需连接的装置是(填序号),该装置中应加入试剂。从实验安全角度考虑,A装置试管中除加入反应液外,还需加入的固体物质是。
(2)若用A装置做乙醇氧化成乙醛的实验,则还应选用的装置是填序号),再用制得的乙醛溶液进行银镜反应,正确的操作顺序是(填序号)。
①向试管中滴入3滴乙醛溶液
②一边振荡一边滴入2%的稀氨水,直至最初产生的沉淀恰好溶解为止
③振荡后放入热水中,水浴加热
④在洁净的试管中加入1mL2%的AgNO3溶液
(14分) 某兴趣小组用下图装置探究氨的催化氧化。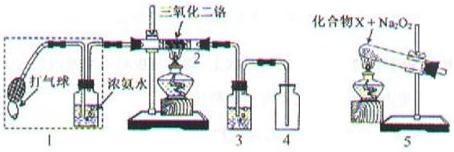
(5)氨催化氧化的化学方程式为________________________________________________。
(6)加热玻璃管2一段时间后,挤压1中打气球鼓入空气,观察到2中物质呈红热状态;停止加热后仍能保持红热,该反应是_________反应(填“吸热”或“放热”)。
(7)为保证在装置4中观察到红棕色气体,装置3应装入_________________;若取消3,在4中仅观察到大量白烟,原因是___________________________________________。
(8)为实现氨催化氧化,也可用装置5替换装置_________(填装置代号);化合物X为_________(只写一种)。
Ⅰ.甲同学利用下列装置验证木炭与浓硫酸反应的全部产物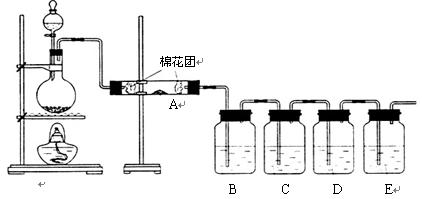
(1)写出木炭与浓硫酸反应的化学方程式:
(2)A中加入的试剂是,B、D中加入的试剂都是品红溶液,D中正确的实验现象是:
(3)实验时,C中若加入的是滴有淀粉的碘水,观察到的现象是,
离子方程式为:。
Ⅱ.乙同学只用B、C、D、E装置验证SO2的某些性质,请回答下列问题:
(1)C中加入的试剂是,证明SO2具有氧化性。
(2)D中加入酸性的KMnO4溶液,证明SO2具有性。
(3)E中加入滴有酚酞的NaOH溶液,证明SO2是性气体。
“酒是陈的香”,是因为酒在储存过程中生成了有香味的乙酸乙酯。在实验室我们可以用如图所示的装置来制取乙酸乙酯。回答下列问题:
(1)写出试管a中发生的化学方程式:
。
(2)试管b中所盛的溶液为 ,其主要作用是。
,其主要作用是。
(3)试管b中的导管要在液面的稍上方,不能插入液面以下,其目的是。
(4)该实验中,若用3mol乙醇和1mol乙酸在浓硫酸作用下加热,充分反应后,能否生成1mol乙酸乙酯?(填“能”或“不能”)原因是
 。(不考虑原料损耗)。
。(不考虑原料损耗)。
有一含NaCl、Na2CO3·10H2O和NaHCO3的混合物,某同学设计如下实验,通过测量反应前后C、D装置质量的变化,测定该混合物中各组 分的质量分数。
分的质量分数。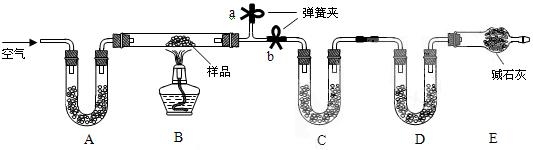
⑴加热前通入空气的目的是 _____________________________________________,操作方 法为______________________________________________。
法为______________________________________________。
⑵装置A、C、D中盛放的试剂分别为A___________,C__________,D__________。
⑶若将A装置换成盛放NaOH溶液的洗气瓶,则测得的NaCl含量将(填“偏高”、“偏低”或“无影响”,下同);若B中反应管右侧有水蒸气冷凝,则测定结果中测定结果中NaHCO3的含量将___________;若撤去E装置,则测得Na2CO3·10H2O的含量__________。
⑷若样品质量为 w g,反应后C、D增加的质量分别为 m1 g、m2 g,由此可知混合物中NaHCO3质量分数为_____________________(用含w、m1、m2的代数式表示)