NA代表阿伏加德罗常数的值,下列有关叙述不正确的是
| A.在熔融状态下,l mol Na2O2完全电离出的离子数目为3 NA |
| B.将CO2通过Na2O2使固体质量增加mg,反应中转移的电子数mNA/14 |
| C.在标准状况下,22.4LCH4与18 gH2O所含有的电子数均为10NA |
| D.含1mol Cl-的NH4Cl溶液中加入适量氨水使溶液呈中性,此时溶液中NH4+数为 NA |
向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如图所示。则下列离子组在对应的溶液中,一定能大量共存的是
| A.a点对应的溶液中:Na+、OH-、SO42-、NO3- |
| B.b点对应的溶液中:Al3+、Fe3+,MnO4-、Cl- |
| C.c点对应的溶液中:Na+、Ca2+、NO3-、Cl- |
| D.d点对应的溶液中:F-、NO3-、Fe2+、Ag+ |
下列说法中,正确的是
| A.用标准盐酸滴定待测氢氧化钠溶液浓度,水洗后的酸式滴定管未经标准液润洗,则滴定结果偏低 |
| B.配制0.1mol/LNaOH溶液时,用潮湿的烧杯称量NaOH固体,对配制结果无影响。 |
| C.测定镀锌铁皮镀层厚度实验,当表面镀层反应完后需将铁皮用水洗,然后用酒精灯高温灼烧冷却后称量,以减少实验误差。 |
| D.测定小苏打中Na2CO3含量的方案:取a(g)样品与足量稀硫酸充分反应,逸出的气体用碱石灰吸收,增重b(g)。 |
有Fe3+、Fe2+、NO3-、NH4+、H+和H2O六种微粒,分别属于一个氧化还原反应中的反应物和生成物,下列叙述中,不正确的是
| A.还原产物为NH4+ |
| B.氧化剂与还原剂的物质的量之比为1∶8 |
| C.若有0.5mol NO3-参加还原反应,则转移电子8mol |
| D.若把该反应设计为电解池,则阳极反应为Fe2+-e→Fe3+ |
常温下Ca(OH)2溶于水达到饱和时存在如下平衡:Ca(OH)2(s) Ca2++2OH-,饱和石灰水的密度为d g/cm3,溶液pH=12。下列有关叙述中,不正确的是
Ca2++2OH-,饱和石灰水的密度为d g/cm3,溶液pH=12。下列有关叙述中,不正确的是
| A.加热至50℃,溶液的Ca2+的浓度增大 |
B.该温度下Ca(OH)2的溶解度为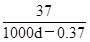 (g/100gH2O) (g/100gH2O) |
| C.该饱和石灰水中,水电离出的OH-的浓度为10-12mol/L |
D.加入生石灰并恢复至常温后,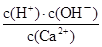 值不变 值不变 |
下列变化能够实现的是:①复分解反应中既没有生成水,也没有生成沉淀和气体;②两种氧化物发生反应有气体生成;③两种酸的溶液充分反应后溶液呈中性;④弱酸与盐溶液反应生成强酸。
| A.只有①③ | B.只有②④ |
| C.只有①②④ | D.①②③④ |